题目内容
下列性质的递变中,正确的是( )A.O、S、Na的原子半径依次增大
B.LiOH、KOH、CsOH的碱性依次增强
C.HF、NH3、SiH4的稳定性依次增强
D.HCl、HBr、HI的还原性依次减弱
答案:AB
解析:
解析:
| 解析:由元素周期表的知识可知:A项O位于第二周期,S、Na属于第三周期,故S、Na的原子半径大于O,又因为S的核电荷数16大于Na的核电荷数11,故Na的原子半径大于S,即三者顺序为O<S<Na,A项正确;B项Li、K、Cs为同一主族元素,随着原子序数的增加,金属性逐渐增强,故有碱性强弱顺序为:LiOH<KOH<CsOH,即B项正确;C项由F、N、Si在元素周期表中的位置可知,它们的非金属性强弱顺序为:F>N>Si,故它们的氢化物稳定性顺序为:HF>NH3>SiH4,C项错误;D项事实上是比较Cl-、Br-、I-的还原性,因Cl-、Br-、I-的半径逐渐增加,故它们失电子的能力逐渐增强,即HCl、HBr、HI的还原性逐渐增强,D项说法错误.
|

练习册系列答案
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案
相关题目
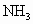 、
、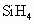 的稳定性依次增强
的稳定性依次增强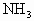 、
、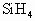 的热稳定性依次增强
的热稳定性依次增强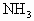 、
、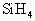 的热稳定性依次增强
的热稳定性依次增强