题目内容
将锌、铜用导线连接后浸入2mol/L的稀硫酸中构成原电池
(1)正极电极反应式为 ,发生 反应(填氧化或还原);电子从 经外电路到 (填锌或铜),溶液中H+向 移动(填正极或负极)
(2)放电一段时间后,正极区pH值 (填变大、变小或不变).当导线中有1mol电子通过时,铜片上析出 升 H2(标准状况下).
(3)利用反应:Fe+2Fe3+=3Fe2+设计一个化学电池(电极材料和电解液自选),画出实验装置图,注明电解质溶液名称和正负极材料.
(1)正极电极反应式为
(2)放电一段时间后,正极区pH值
(3)利用反应:Fe+2Fe3+=3Fe2+设计一个化学电池(电极材料和电解液自选),画出实验装置图,注明电解质溶液名称和正负极材料.
考点:设计原电池,原电池和电解池的工作原理
专题:电化学专题
分析:用锌片、铜片连接后浸入稀硫酸溶液中,构成了原电池,锌为负极,电极反应为:Zn-2e-=Zn2+;铜为正极,电极反应为2H++2e-=H2↑;根据两极转移电子数目相等计算;根据反应Fe+2Fe3+=3Fe2+可知Fe应为负极,被氧化,正极可为C、Cu等,电解质溶液含有Fe3+.
解答:
解:(1)锌比铜活泼,形成原电池反应时,锌为负极,铜为正极,正极发生还原反应,电极方程式为2H++2e-=H2↑,原电池工作时,电子从锌极经导线流向铜极,溶液中阳离子向正极移动,
故答案为:2H++2e-=H2↑;还原;锌;铜;正极;
(2)正极反应为2H++2e-=H2↑,可知放电一段时间后,正极区pH值变大,当导线中有1mol电子通过时,铜片上析出0.5mol氢气,体积为11.2L,
故答案为:变大;11.2;
(3)根据反应可知Fe应为负极,被氧化,正极可为C、Cu等,电解质溶液含有Fe3+,乐为氯化铁或硫酸铁等,装置图为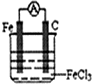 ,
,
故答案为: .
.
故答案为:2H++2e-=H2↑;还原;锌;铜;正极;
(2)正极反应为2H++2e-=H2↑,可知放电一段时间后,正极区pH值变大,当导线中有1mol电子通过时,铜片上析出0.5mol氢气,体积为11.2L,
故答案为:变大;11.2;
(3)根据反应可知Fe应为负极,被氧化,正极可为C、Cu等,电解质溶液含有Fe3+,乐为氯化铁或硫酸铁等,装置图为
 ,
,故答案为:
 .
.
点评:本题考查较为综合,涉及原电池的设计和工作原理的探究,为高考常见题型,侧重于基础知识的考查,题目难度不大,注意把握原电池的组成和原理,学习中注意基础知识的积累.

练习册系列答案
 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案
相关题目
 下列反应过程中的能量变化与图一致的是( )
下列反应过程中的能量变化与图一致的是( )A、2Al+Fe2O3
| ||||
B、C+CO2
| ||||
C、CaCO3
| ||||
D、C+H2O
|
下列叙述中正确的是( )
| A、牛油是纯净物,它不属于高分子 |
| B、牛油是高级脂肪酸的高级醇酯 |
| C、牛油可以在碱性条件下加热水解 |
| D、工业上将牛油加氢制造硬化油 |
19.2mg铜与一定量的浓硝酸反应,铜全部反应后,共收集到气体11.2mL(标准状况),反应消耗硝酸的物质的量是( )
| A、0.5×10-3 mol |
| B、0.8×10-3 mol |
| C、1.1×10-3 mol |
| D、1.2×10-3 mol |
在物质分类中,前者包括后者的是( )
| A、氧化物、化合物 |
| B、化合物、酸性氧化物 |
| C、溶液、胶体 |
| D、溶液、分散系 |

