题目内容
15.锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子通过,下列有关叙述正确的是( )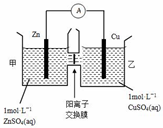
| A. | 电池工作一段时间后,乙池溶液的总质量增加 | |
| B. | 电池工作一段时间后,甲池的c(SO42-)减小 | |
| C. | 铜电极上发生氧化反应 | |
| D. | 阴阳离子分别通过交换膜向负极和正极移动,保持溶液中电荷平衡 |
分析 由图象可知,该原电池反应式为:Zn+Cu2+=Zn2++Cu,Zn发生氧化反应,为负极,Cu电极上发生还原反应,为正极,阳离子交换膜只允许阳离子和水分子通过,两池溶液中硫酸根浓度不变,随反应进行,甲池中的Zn2+通过阳离子交换膜进入乙池,以保持溶液呈电中性,进入乙池的Zn2+与放电的Cu2+的物质的量相等,而Zn的摩尔质量大于Cu,故乙池溶液总质量增大,以此解答该题.
解答 解:A.甲池中的Zn2+通过阳离子交换膜进入乙池,乙池中发生反应:Cu2++2e-=Cu,保持溶液呈电中性,进入乙池的Zn2+与放电的Cu2+的物质的量相等,而Zn的摩尔质量大于Cu,故乙池溶液总质量增大,故A正确;
B.阳离子交换膜只允许阳离子和水分子通过,故两池中c(SO42-)不变,故B错误;
C.锌为负极,铜为正极,正极上铜离子得电子发生还原反应,故C错误;
D.阳离子交换膜只允许阳离子通过,阴离子不能通过阳离子交换膜,故D错误.
故选A.
点评 本题考查原电池工作原理,侧重于学生的分析能力的考查,注意把握原电池的工作原理,题目比较基础,注意阳离子交换膜不允许阳离子通过,D选项利用电荷守恒分析.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.使1mol某烷烃完全燃烧需要消耗氧气5mol,该烷烃的化学式是( )
| A. | C2H6 | B. | C3H8 | C. | C4H10 | D. | C5H12 |
3.25℃把 0.02mol/LCH3COOH溶液和0.01mol/LKOH溶液以等体积混和,则混合液中微粒浓度关系正确的为:(已知?25℃:CH3COOH电离常数是1.76×10-5,CH3COO-水解常数是5.78×10-10;?体积变化忽略不计;)( )
| A. | c (K+)>c (CH3COO-)>c(H+)>c (OH-) | B. | c(K+)=c (CH3COO-)>c (OH-)=c (H+) | ||
| C. | c(K+)+c (H+)═c(CH3COOH)+c (OH-) | D. | c (CH3COOH)+c (CH3COO-)=0.01mol/L |
10.盐酸或硫酸和氢氧化钠溶液的中和反应没有明显的现象.某学习兴趣小组的同学为了证明氢氧化钠溶液与盐酸或硫酸发生了反应,从中和反应的热效应出发,设计了下面几种实验方案.请回答有关问题.
(1)方案一:如图1装好实验装置,图中小试管用细线吊着,细线的上端拴在细铁丝上.开始时使右端U形管两端红墨水相平.实验开始,向下插细铁丝,使小试管内盐酸和广口瓶内氢氧化钠溶液混合,此时观察到的现象是U形管内液面左边下降、右边升高,原因是盐酸和氢氧化钠发生中和反应放出热量,使瓶内气体温度升高,压强增大.

(2)方案二:该小组借助反应溶液温度的变化来判断反应的发生.如果氢氧化钠溶液与盐酸混合前后有温度的变化,则证明发生了化学反应.该小组同学将不同浓度的氢氧化钠溶液和盐酸各10mL混合,用温度计测量反应前后温度的变化,测得的部分数据如下表:
则x=7.
(3)方案三:该小组还设计了如图2示装置来证明氢氧化钠溶液确实与稀硫酸发生了反应.他们认为若洗气瓶中导管口有气泡冒出,则说明该反应放出热量,从而证明发生了反应.
①实验时,打开分液漏斗活塞,发现导管流出液体不畅,原因可能是没打开分液漏斗上部塞子
②从原理上讲,该实验设计的不合理之处为稀硫酸具有一定的体积,冒出气泡的原因可能是加入稀硫酸的体积引起的.
请你在此实验装置的基础上提出修改方案分液漏斗上口和锥形瓶之间连接一导管.
(1)方案一:如图1装好实验装置,图中小试管用细线吊着,细线的上端拴在细铁丝上.开始时使右端U形管两端红墨水相平.实验开始,向下插细铁丝,使小试管内盐酸和广口瓶内氢氧化钠溶液混合,此时观察到的现象是U形管内液面左边下降、右边升高,原因是盐酸和氢氧化钠发生中和反应放出热量,使瓶内气体温度升高,压强增大.

(2)方案二:该小组借助反应溶液温度的变化来判断反应的发生.如果氢氧化钠溶液与盐酸混合前后有温度的变化,则证明发生了化学反应.该小组同学将不同浓度的氢氧化钠溶液和盐酸各10mL混合,用温度计测量反应前后温度的变化,测得的部分数据如下表:
| 编号 | 盐酸 | 氢氧化钠 | △t/℃ |
| 1 | 0.1mol•L-1 | 0.05mol•L-1 | 3.5 |
| 2 | 0.1mol•L-1 | 0.1mol•L-1 | x |
| 3 | 0.2mol•L-1 | 0.2mol•L-1 | 14 |
(3)方案三:该小组还设计了如图2示装置来证明氢氧化钠溶液确实与稀硫酸发生了反应.他们认为若洗气瓶中导管口有气泡冒出,则说明该反应放出热量,从而证明发生了反应.
①实验时,打开分液漏斗活塞,发现导管流出液体不畅,原因可能是没打开分液漏斗上部塞子
②从原理上讲,该实验设计的不合理之处为稀硫酸具有一定的体积,冒出气泡的原因可能是加入稀硫酸的体积引起的.
请你在此实验装置的基础上提出修改方案分液漏斗上口和锥形瓶之间连接一导管.
7.下列反应的离子方程式正确的是( )
| A. | 硫酸铜与烧碱溶液反应:CuSO4+2OH-═Cu(OH)2↓+SO42- | |
| B. | 钠与水反应:Na+2H2O═Na++2OH-+H2↑ | |
| C. | 碳酸钠溶液中加入足量盐酸:Na2CO3+2H+═Na++CO2↑+H2O | |
| D. | 氢氧化铝中和胃酸(盐酸):Al(OH)3+3H+═Al3++3H2O |
4.图是石油分馏塔的示意图,a、b、c三种馏分中( )
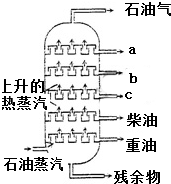

| A. | a的沸点最高 | B. | b的熔点最低 | ||
| C. | c的碳原子数最多 | D. | 每一种馏分都是纯净物 |
 实验室要配制2mol/L稀硫酸250mL.
实验室要配制2mol/L稀硫酸250mL.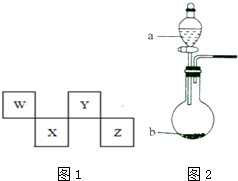 W、X、Y、Z四种短周期元素在周期表中的位置如图1所示,其中Y与钠元素和氢元素均可形成原子个数1:1和1:2的化合物.
W、X、Y、Z四种短周期元素在周期表中的位置如图1所示,其中Y与钠元素和氢元素均可形成原子个数1:1和1:2的化合物.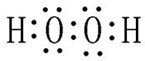 ,Z在周期表中的位置第三周期ⅦA族.
,Z在周期表中的位置第三周期ⅦA族. ;取代反应
;取代反应 ;加成反应
;加成反应 ;取代反应
;取代反应