题目内容
 已知R-CH═CH2+HX
已知R-CH═CH2+HX| Au |
 .如图中的A、B分别是分子式为C3H7Cl的两种同分异构体,请根据图中所示物质转化关系和反应条件,判断并写出:
.如图中的A、B分别是分子式为C3H7Cl的两种同分异构体,请根据图中所示物质转化关系和反应条件,判断并写出:(1)写出下列物质的结构简式
A、
(2)①写出由E转化为B化学方程式
②写出由C转化为E的化学方程式
考点:有机物的推断
专题:有机物的化学性质及推断
分析:C3H7Cl的两种同分异构体分别为CH3CH2CH2Cl和 ,A不论是二者中的哪一种结构,当在NaOH醇溶液中发生反应时只生成一种结构:CH3CH=CH2,即E为CH3CH=CH2,根据题目所给信息可知B为
,A不论是二者中的哪一种结构,当在NaOH醇溶液中发生反应时只生成一种结构:CH3CH=CH2,即E为CH3CH=CH2,根据题目所给信息可知B为 ,则A为CH3CH2CH2Cl,进一步可知C为CH3CH2CH2OH,D为
,则A为CH3CH2CH2Cl,进一步可知C为CH3CH2CH2OH,D为 ,结合有机物的结构和性质以及题目要求可解答该题.
,结合有机物的结构和性质以及题目要求可解答该题.
 ,A不论是二者中的哪一种结构,当在NaOH醇溶液中发生反应时只生成一种结构:CH3CH=CH2,即E为CH3CH=CH2,根据题目所给信息可知B为
,A不论是二者中的哪一种结构,当在NaOH醇溶液中发生反应时只生成一种结构:CH3CH=CH2,即E为CH3CH=CH2,根据题目所给信息可知B为 ,则A为CH3CH2CH2Cl,进一步可知C为CH3CH2CH2OH,D为
,则A为CH3CH2CH2Cl,进一步可知C为CH3CH2CH2OH,D为 ,结合有机物的结构和性质以及题目要求可解答该题.
,结合有机物的结构和性质以及题目要求可解答该题.解答:
解:C3H7Cl的两种同分异构体分别为CH3CH2CH2Cl和 ,A不论是二者中的哪一种结构,当在NaOH醇溶液中发生反应时只生成一种结构:CH3CH=CH2,即E为CH3CH=CH2,根据题目所给信息可知B为
,A不论是二者中的哪一种结构,当在NaOH醇溶液中发生反应时只生成一种结构:CH3CH=CH2,即E为CH3CH=CH2,根据题目所给信息可知B为 ,则A为CH3CH2CH2Cl,进一步可知C为CH3CH2CH2OH,D为
,则A为CH3CH2CH2Cl,进一步可知C为CH3CH2CH2OH,D为 ,
,
(1)由以上分析可知A为CH3CH2CH2Cl,D为 ,故答案为:CH3CH2CH2Cl;
,故答案为:CH3CH2CH2Cl; ;
;
(2)①由E转化为B化学方程式为CH3CH=CH2+HCl
 ,②C为CH3CH2CH2OH,可在浓硫酸作用下加热发生消去反应生成CH3CH=CH2,反应的方程式为CH3CH2CH2OH
,②C为CH3CH2CH2OH,可在浓硫酸作用下加热发生消去反应生成CH3CH=CH2,反应的方程式为CH3CH2CH2OH
CH3CH=CH2+H2O,该反应为消去反应,
故答案为:CH3CH=CH2+HCl
 ;CH3CH2CH2OH
;CH3CH2CH2OH
CH3CH=CH2+H2O;消去反应.
 ,A不论是二者中的哪一种结构,当在NaOH醇溶液中发生反应时只生成一种结构:CH3CH=CH2,即E为CH3CH=CH2,根据题目所给信息可知B为
,A不论是二者中的哪一种结构,当在NaOH醇溶液中发生反应时只生成一种结构:CH3CH=CH2,即E为CH3CH=CH2,根据题目所给信息可知B为 ,则A为CH3CH2CH2Cl,进一步可知C为CH3CH2CH2OH,D为
,则A为CH3CH2CH2Cl,进一步可知C为CH3CH2CH2OH,D为 ,
,(1)由以上分析可知A为CH3CH2CH2Cl,D为
 ,故答案为:CH3CH2CH2Cl;
,故答案为:CH3CH2CH2Cl; ;
;(2)①由E转化为B化学方程式为CH3CH=CH2+HCl
| Au |
 ,②C为CH3CH2CH2OH,可在浓硫酸作用下加热发生消去反应生成CH3CH=CH2,反应的方程式为CH3CH2CH2OH
,②C为CH3CH2CH2OH,可在浓硫酸作用下加热发生消去反应生成CH3CH=CH2,反应的方程式为CH3CH2CH2OH| 浓硫酸 |
| △ |
故答案为:CH3CH=CH2+HCl
| Au |
 ;CH3CH2CH2OH
;CH3CH2CH2OH| 浓硫酸 |
| △ |
点评:本题考查有机物的推断,题目难度不大,本题注意以E为突破口结合题目信息推断,明确同分异构体的判断为解答该题的关键,注意把握有机物的官能团的结构和性质.

练习册系列答案
 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案
相关题目
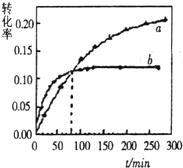 丙酮(CH3COCH3)在某溶剂里,在催化剂作用下发生反应:2CH3COCH3(aq)?CH3COCH2COH(CH3)2(aq)取相同浓度的CH3COCH3,分别在40℃和60℃时,测得其转化率α随时间变化的关系曲线(α-t)如图所示.下列说法正确的是( )
丙酮(CH3COCH3)在某溶剂里,在催化剂作用下发生反应:2CH3COCH3(aq)?CH3COCH2COH(CH3)2(aq)取相同浓度的CH3COCH3,分别在40℃和60℃时,测得其转化率α随时间变化的关系曲线(α-t)如图所示.下列说法正确的是( )| A、b代表40℃时CH3COCH3的α-t曲线 |
| B、升高温度可缩短该反应达平衡的时间并能提高平衡转化率 |
| C、增大压强可缩短该反应达平衡的时间并能提高平衡转化率 |
| D、上述反应的逆反应为吸热反应 |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、在0.1 mol?L-1 NaOH溶液中:K+、Na+、SO42-、HCO3- |
| B、在c( H+)/c(OH-)=10-12的溶液中:K+、Na+、ClO-、NO3- |
| C、在0.1 mol?L-1 FeCl3溶液中:K+、NH4+、I-、SCN- |
| D、在0.1 mol?L-1 Na2CO3溶液中:Al3+、Ba2+、NO3-、Cl- |
Cl2、SO2均能使品红溶液褪色.后者因为品红分子结构中的发色团遇到亚硫酸后结构发生改变,生成不稳定的无色化合物.其漂白原理可用下面的反应方程式表示.下列说法正确的是( )

| A、品红溶液中同时通入Cl2、SO2,漂白效果会更好 |
| B、加热可判断品红褪色是通入SO2还是通入Cl2引起的 |
| C、“无色化合物”分子中,19个碳原子都可能在同一平面上 |
| D、品红属于芳香烃 |
把一定量的铁粉放入氯化铁溶液中,充分反应后所得溶液中Fe3+和Fe2+的浓度恰好相等,则反应的铁和未反应的Fe3+的物质的量之比为( )
| A、1:3 | B、1:2 |
| C、1:1 | D、3:1 |
决定主族元素在周期表中的位置的是( )
| A、质量数和质子数 |
| B、质子数和中子数 |
| C、电子层数和最外层电子数 |
| D、主要化合价 |
