题目内容
19.某食品袋中有一个写着“干燥剂”的小纸袋,里面的主要成分是生石灰,对此“干燥剂”的说法正确的是( )| A. | 小纸袋中的物质可长期持续地做干燥剂 | |
| B. | 生石灰属于盐类 | |
| C. | 此干燥剂为混合物 | |
| D. | 其中钙元素的存在形态为游离态 |
分析 A.氧化钙吸水后生成氢氧化钙后不能继续做干燥剂;
B.生石灰含有钙、氧两种元素;
C.“干燥剂”的小纸袋,里面的主要成分是生石灰属于混合物;
D.干燥剂中是氧化钙,钙元素是化合态.
解答 解:A.氧化钙吸水后生成氢氧化钙,失去吸水的作用,不能继续做干燥剂,故A错误;
B.生石灰含有钙、氧两种元素属于氧化物,故B错误;
C.“干燥剂”的小纸袋,里面的主要成分是生石灰属于混合物,故C正确;
D.干燥剂中是氧化钙,钙元素是化合态,故D错误;
故选:C.
点评 本题考查了干燥剂的组成和性质分析,明确干燥剂成分及性质是解题关键,题目较简单.

练习册系列答案
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案
相关题目
14.在托盘天平两端各放一只烧杯,调节至平衡.在两只烧杯里加入等质量、等质量分数的稀盐酸,然后再左右两烧杯中分别放入质量相等的镁和铝,带充分反应后,镁有剩余,则还可以观察到的现象是( )
①天平保持平衡 ②铝也有剩余 ③天平指针偏向放镁的一方 ④天平指针偏向放铝的一方.
①天平保持平衡 ②铝也有剩余 ③天平指针偏向放镁的一方 ④天平指针偏向放铝的一方.
| A. | 只有① | B. | ①和② | C. | ②和④ | D. | 只有③ |
4.如图是探究铜丝与过量浓硫酸的反应,下列叙述不正确的是( )
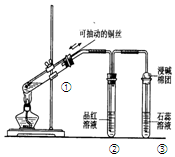

| A. | 上下移动①中铜丝可控制SO2的量 | |
| B. | ②中品红溶液褪色 | |
| C. | ③中石蕊溶液变红色 | |
| D. | 为确认CuSO4生成,向①中加水,观察溶液颜色 |
11.NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 在常温常压下,11.2 L N2含有的分子数为0.5NA | |
| B. | 在标准状况下,11.2 L H2O所含的分子数为0.5NA | |
| C. | 在常温常压下,1 mol O2含有的原子数为2NA | |
| D. | 只有在标准状况下的气体摩尔体积才是22.4L/mol. |
8.实验室常利用以下反应制取少量氮气:NaNO2+NH4Cl═NaCl+N2↑+2H2O关于该反应的下列说法正确的是( )
| A. | N2既是氧化剂,又是还原剂 | |
| B. | NaNO2是氧化剂,氧化产物、还原产物都是N2 | |
| C. | NH4Cl中的氮元素被还原 | |
| D. | 每生成1 mol N2时,转移电子的物质的量为6 mol |
9.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 0.1 molCl2与足量Fe反应转移电子数为0.3NA | |
| B. | 标况下,11.2L 氟化氢中含有的分子数目为0.5NA | |
| C. | 常温常压下,4.2g环丙烷和聚乙烯的混合物中含有的碳原子数为0.3 NA | |
| D. | 25℃,pH=13的NaOH溶液中含有OH-的数目为0.1NA |
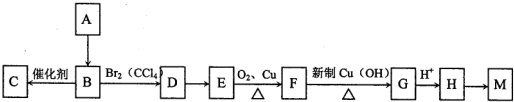
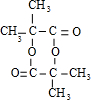 .
.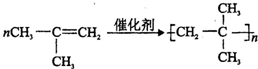 ;E→F
;E→F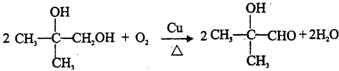 .
.