题目内容
1.为除去粗盐中的Ca2+、Mg2+、SO${\;}_{4}^{2-}$以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):称取粗盐$→_{①}^{溶解}$$→_{②}^{BaCl_{2}}$$→_{③}^{NaOH}$$→_{④}^{Na_{2}CO_{3}}$$→_{⑤}^{过滤}$滤液$→_{⑥}^{适量盐酸}$$→_{⑦}^{蒸发、结晶、烘干}$精盐
(1)第⑤步实验操作需要烧杯、漏斗、玻璃棒等玻璃仪器.
(2)第⑥步中,有关反应的离子方程式是OH-+H+=H2O、CO32-+2H+=H2O+CO2↑.
分析 除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,加水溶解后,盐酸要放在最后,用于除去过量的氢氧化钠和碳酸钠,要先加过量的氯化钡除去硫酸根离子,然后用碳酸钠去除过量的钡离子,即必须满足碳酸钠溶液应该在加入氯化钡溶液之后,盐酸必须在过滤之后加入,则②中加氯化钡可除去硫酸根离子,③中加NaOH除去镁离子,④中加碳酸钠可除去钡离子、钙离子,过滤后主要为氯化钠和碳酸钠,⑥中加盐酸反应后溶液中溶质为NaCl,然后蒸发结晶(剩余少量液体停止加热)得到NaCl,以此解答该题.
解答 解:由流程可知,②中加氯化钡可除去硫酸根离子,③中加NaOH除去镁离子,④中加碳酸钠可除去钡离子、钙离子,过滤后主要为氯化钠和碳酸钠,⑥中加盐酸反应后溶液中溶质为NaCl,然后蒸发结晶得到NaCl,
(1)第⑤步为过滤操作,实验操作需要烧杯、漏斗、玻璃棒等玻璃仪器,故答案为:漏斗;玻璃棒;
(2)过滤得到滤液中含有氯化钠、过量氢氧化钠、碳酸钠,第⑥步中需要加入适量盐酸到不再有气体生成证明除去氢氧化钠和碳酸钠,反应的离子方程式为:OH-+H+=H2O、CO32-+2H+=H2O+CO2↑,
故答案为:OH-+H+=H2O、CO32-+2H+=H2O+CO2↑.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、混合物分离方法为解答的关键,侧重分析与实验能力的考查,注意离子检验及沉淀的洗涤,题目难度不大.

练习册系列答案
 综合自测系列答案
综合自测系列答案
相关题目
19.下列反应的离子方程式书写正确的是( )
| A. | 稀醋酸与氢氧化钠溶液的反应:H++OH-=H2O | |
| B. | 钠与水反应:Na+H2O=Na++OH-+H2↑ | |
| C. | 氯气与氯化亚铁溶液的反应:Cl2+2Fe2+=2Cl-+2Fe3+ | |
| D. | 碳酸钙溶液与足量稀盐酸的反应:CO32-+2H+=H2O+CO2↑ |
6.中美科学家研制的某快充电池工作原理如图所示.电解质为一种常温离子液体(由有机阳离子、Al2Cl7-和AlCl4-组成),在电池充、放电过程中,不产生其他离子且有机阳离子不参与电极反应.下列有关该快充电池的说法错误的是( )
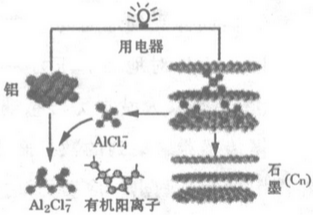

| A. | 放电时铝为电池阳极 | |
| B. | 充电时AlCl4-移向石墨电极 | |
| C. | 铝电极的比能量较高 | |
| D. | 充电时铝电极上的反应为Al+7AlCl4--3e-=4Al2Cl7- |
10. 苯甲酸乙酯(C9H10O2)是一种无色透明液体,不溶于水,稍有水果香味,用于配制香水香精和人造精油,大量用于食品工业中,也可用作有机合成中间体,溶剂等.
苯甲酸乙酯(C9H10O2)是一种无色透明液体,不溶于水,稍有水果香味,用于配制香水香精和人造精油,大量用于食品工业中,也可用作有机合成中间体,溶剂等.
(1)其制备方法为:
(2)已知:①
②苯甲酸在100℃会迅速升华
③无水氯化钙可与乙醇形成难溶于水的CaCl2•6C2H5OH
(3)实验步骤如下:
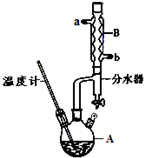
①在仪器A中加入12.20g苯甲酸,25mL 95%的乙醇(过量),20mL环己烷以及4mL浓硫酸,混合均匀并加入沸石,按如图所示装好仪器,控制温度在65~70℃加热回流2h.利用分水器不断分离除去反应生成的水,回流环己烷和乙醇.
②反应结束,打开旋塞放出分水器中液体后,关闭旋塞,继续加热,至分水器中收集到的液体不再明显增加,停止加热.
③将仪器A内反应液倒入盛有适量水的烧杯中,分批加入Na2CO3至溶液呈中性.用分液漏斗分出有机层,水层用25mL乙醚萃取分液,然后合并至有机层,加入氯化钙,静置,过滤,将滤液用蒸馏烧瓶进行分馏,低温蒸出乙醚和环己烷后,继续升温,接收210~213℃的馏分.
④检验合格,测得产品体积为12.86mL.
回答下列问题:
(1)在该实验中,仪器A的名称为三颈烧瓶,其容积最适合的是C(填选项前的字母).
A.25mL B.50mL C.100mL D.250mL
(2)制备苯甲酸乙酯时,最合适的加热方法是水浴加热,控制温度的目的是防止副反应的发生和苯甲酸升华.加入沸石的作用是防暴.
(3)步骤①中使用分水器不断分离除去水的目的是使平衡不断地向正向移动.
(4)步骤②中应控制馏分的温度在C.
A.65~70℃B.78~80℃C.85~90℃D.215~220℃
(5)步骤③有机层应从分液漏斗下口(填“上口”或“下口”)流出.加入Na2CO3的作用是除去硫酸和未反应的苯甲酸;若Na2CO3加入不足,在之后蒸馏时,蒸馏烧瓶中可见到白烟生成,产生该现象的原因是苯甲酸乙酯中混有未除净的苯甲酸,在受热至100℃时发生升华.加入氯化钙的目的是使产品中混有的乙醇形成难溶于水的CaCl2•6C2H5OH,过滤除去.
(6)计算本实验的产率为90.02%.
 苯甲酸乙酯(C9H10O2)是一种无色透明液体,不溶于水,稍有水果香味,用于配制香水香精和人造精油,大量用于食品工业中,也可用作有机合成中间体,溶剂等.
苯甲酸乙酯(C9H10O2)是一种无色透明液体,不溶于水,稍有水果香味,用于配制香水香精和人造精油,大量用于食品工业中,也可用作有机合成中间体,溶剂等.(1)其制备方法为:

(2)已知:①
| 名称 | 相对分子质量 | 颜色,状态 | 沸点(℃) | 密度(g•cm-3) |
| 苯甲酸 | 122 | 无色片状晶体 | 249 | 1.2659 |
| 苯甲酸乙酯 | 150 | 无色澄清液体 | 212.6 | 1.05 |
| 乙醇 | 46 | 无色澄清液体 | 78.3 | 0.7893 |
| 环己烷 | 84 | 无色澄清液体 | 80.8 | 0.7318 |
③无水氯化钙可与乙醇形成难溶于水的CaCl2•6C2H5OH
(3)实验步骤如下:
①在仪器A中加入12.20g苯甲酸,25mL 95%的乙醇(过量),20mL环己烷以及4mL浓硫酸,混合均匀并加入沸石,按如图所示装好仪器,控制温度在65~70℃加热回流2h.利用分水器不断分离除去反应生成的水,回流环己烷和乙醇.
②反应结束,打开旋塞放出分水器中液体后,关闭旋塞,继续加热,至分水器中收集到的液体不再明显增加,停止加热.
③将仪器A内反应液倒入盛有适量水的烧杯中,分批加入Na2CO3至溶液呈中性.用分液漏斗分出有机层,水层用25mL乙醚萃取分液,然后合并至有机层,加入氯化钙,静置,过滤,将滤液用蒸馏烧瓶进行分馏,低温蒸出乙醚和环己烷后,继续升温,接收210~213℃的馏分.
④检验合格,测得产品体积为12.86mL.
回答下列问题:
(1)在该实验中,仪器A的名称为三颈烧瓶,其容积最适合的是C(填选项前的字母).
A.25mL B.50mL C.100mL D.250mL
(2)制备苯甲酸乙酯时,最合适的加热方法是水浴加热,控制温度的目的是防止副反应的发生和苯甲酸升华.加入沸石的作用是防暴.
(3)步骤①中使用分水器不断分离除去水的目的是使平衡不断地向正向移动.
(4)步骤②中应控制馏分的温度在C.
A.65~70℃B.78~80℃C.85~90℃D.215~220℃
(5)步骤③有机层应从分液漏斗下口(填“上口”或“下口”)流出.加入Na2CO3的作用是除去硫酸和未反应的苯甲酸;若Na2CO3加入不足,在之后蒸馏时,蒸馏烧瓶中可见到白烟生成,产生该现象的原因是苯甲酸乙酯中混有未除净的苯甲酸,在受热至100℃时发生升华.加入氯化钙的目的是使产品中混有的乙醇形成难溶于水的CaCl2•6C2H5OH,过滤除去.
(6)计算本实验的产率为90.02%.
11.下列名称的有机物实际上不可能存在的是( )
| A. | 2,2-二甲基丁烷 | B. | 3-甲基-1-丁炔 | ||
| C. | 3-甲基-2-戊烯 | D. | 3,3-二甲基-2-戊烯 |

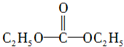 .
.

