题目内容
等体积、等物质的量浓度的Na2SO4和Na2CO3溶液中,阴阳离子总数相比( )
| A、前者多 | B、后者多 |
| C、一样多 | D、无法判断 |
考点:离子浓度大小的比较
专题:
分析:根据n=cV可知,等体积、等物质的量浓度Na2SO4和Na2CO3溶液中含有的Na2SO4和Na2CO3的物质的量相等,根据碳酸根离子水解导致溶液阴离子总数增多进行解答.
解答:
解:等体积等物质的量浓度的Na2CO3和Na2SO4溶液中,碳酸钠水解,CO32-+H2O?HCO3-+OH-、HCO3-+H2O?H2CO3+OH-,阴离子数增多,所以Na2SO4溶液中的离子总数小于Na2CO3溶液,
故选B.
故选B.
点评:本题考查了溶液中离子浓度大小比较,题目难度不大,侧重考查盐的水解原理及其应用,注意掌握判断溶液中离子浓度大小的常用方法,明确盐的水解原理为解答本题的关键.

练习册系列答案
相关题目
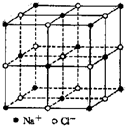 食盐晶体如图所示.在晶体中,?表示Na+,ο 表示Cl-.已知食盐的密度为ρg/cm3,NaCl摩尔质量Mg/mol,阿伏加德罗常数为N,则在食盐晶体里Na+和Cl-的间距大约是( )
食盐晶体如图所示.在晶体中,?表示Na+,ο 表示Cl-.已知食盐的密度为ρg/cm3,NaCl摩尔质量Mg/mol,阿伏加德罗常数为N,则在食盐晶体里Na+和Cl-的间距大约是( )A、
| |||||
B、
| |||||
C、
| |||||
D、
|
下列有关实验原理、方法和结论都正确的是( )
| A、向溶液X中先滴加稀硝酸,再滴加Ba(NO3)2溶液,出现白色沉淀说明溶液X中一定含有SO42- |
| B、取少量溶液X,向其中加入适量新制氯水,再加几滴KSCN溶液,溶液变红,说明X溶液中一定含有Fe2+ |
| C、粗略配制浓度为2mol?L-1的NaCl溶液,可将58.5g NaCl加入到盛有500mL水的烧杯中,搅拌、溶解 |
| D、对某固体进行焰色反应实验,火焰呈黄色,说明该物质为一定钠盐 |
下列各项操作错误的是( )
| A、用酒精萃取溴水中的溴单质的操作可选用分液漏斗,而后静置分液 |
| B、分液时,分液漏斗下层液体从下口放出,上层液体从上口到出 |
| C、萃取,分液前需对分液漏斗检漏 |
| D、为保证分液漏斗内的液体顺利流出,需将上面的塞子拿下 |
下列有关实验原理、操作或现象不正确的是( )
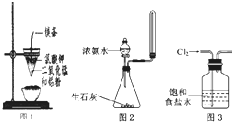

| A、图1装置可制得金属锰,用同样的装置可制得金属铬 |
| B、实验室用图2所示装置制取少量纯净的氨气 |
| C、用玻璃棒蘸取某溶液做焰色反应实验,火焰呈黄色不能说明该溶液中含有钠元素 |
| D、实验室用图3所示装置除去Cl2中的少量HCl |
在一次化学实验操作考核中,某班同学有如下几种操作和应急措施,其中不正确的是( )
A、 酒精失火用湿抹布扑盖 |
B、 将NaCl倒入量筒中配制溶液 |
C、 研磨闻气味鉴别挥发性固体 |
D、 分离溶液中析出的KNO3晶体 |
下列各组有机物中,只需加入溴水就能一一鉴别的是( )
| A、苯、已炔、已烯 |
| B、已烯、苯、四氯化碳 |
| C、已烷、苯、环已烷 |
| D、甲苯、已烷、已烯 |
在下列各组物质中,一定互为同系物的是( )
| A、符合通式CnH2n+2,且相对分子质量不相等的两种有机化合物 |
| B、符合通式CnH2n-2,且相对分子质量不相等的两种有机化合物 |
| C、符合通式CnH2n-6,且相对分子质量不相等的两种有机化合物 |
| D、符合通式CnH2n,且相对分子质量不相等的两种有机化合物 |