题目内容
15.所含电子总数相等的微粒叫等电子体,下列各组微粒属于等电子体的是( )| A. | HCl和F2 | B. | NO和CO | C. | NH2-和NH4+ | D. | CH4和H2S |
分析 根据题目信息,电子数目相同的微粒为等电子体,粒子中质子数等于原子的质子数之和,中性微粒中质子数=电子数,阳离子的电子数=质子数-电荷数,阴离子的电子数=质子数+电荷数,据此结合选项判断.
解答 解:A.HCl的核外电子总数为17+1=,F2的核外电子数总数也是9×2=18,二者含有的电子数相同,属于等电子体,故A正确;
B.NO的核外电子总数为15,CO的核外电子总数14,二者电子数不相同,故B错误;
C.NH2-的电子数为7+1×2+1=10,NH4+的电子数为7+1×4-1=10,二者电子数相同,故C正确;
D.CH4的电子数为6+4=10,H2S的电子数为1×2+16=18,二者电子数不相同,故D错误;
故选AC.
点评 本题主要考查等电子体的判断,题目难度不大,明确题干信息的含义为解答关键,试题侧重基础知识的考查,培养了想的分析、理解能力.

练习册系列答案
相关题目
5.下列电离方程式或离子方程式中,书写正确的是( )
| A. | NaHCO3→Na++H++CO32- | B. | HClO→H++ClO- | ||
| C. | H2S?2H++S2- | D. | NH4++OH-→NH3•H2O |
6.与50mL0.1moL/LNa2CO3溶液中的钠离子的物质的量浓度相同的溶液是( )
| A. | 50mL0.2moL/L的NaCl溶液 | B. | 100mL0.1moL/L的NaCl溶液 | ||
| C. | 25mL0.2moL/L的Na2SO4溶液 | D. | 10mL0.5moL/L的Na2CO3溶液 |
10.25℃某气态烃与氧气混合充入密闭容器中,点火爆炸后,恢复到25℃,此时容器内压强为开始时的一半,再经氢氧化钠溶液处理后,容器内几乎为真空,该烃的分子式为( )
| A. | C2H4 | B. | C2H6 | C. | C3H4 | D. | C3H6 |
20.下列说法中正确的是( )
| A. | 等物质的量浓度的(NH4)2CO3溶液和(NH4)2SO4溶液中c(NH4+)相同 | |
| B. | FeCl3溶液不能与固体CaCO3发生反应 | |
| C. | 一定条件下,反应2Mg(s)+CO2(g)═C(s)+2MgO(s)具有自发性,其△H>0 | |
| D. | 将0.005mol Na2O2溶于水得到1L溶液,此溶液在常温下的pH=12 |
19.根据碘与氢气反应的热化学方程式判断正确的是( )
①I2(g)+H2(g)?2HI(g)+Q1
②I2(s)+H2(g)?2HI(g)-Q2.
①I2(g)+H2(g)?2HI(g)+Q1
②I2(s)+H2(g)?2HI(g)-Q2.
| A. | 1mol I2(g)与1mol H2(g)充分反应放热Q1 kJ | |
| B. | 1mol气态碘与1mol固态碘所含的能量相差(Q1+Q2)kJ | |
| C. | 反应①的生成物总能量比反应②的生成物总能量高 | |
| D. | 稳定性:I2(g)>I2(s) |
20.分离混合物的方法错误的是( )
| A. | 分离苯和硝基苯:蒸馏 | B. | 分离氯化钠与氯化铵固体:升华 | ||
| C. | 分离水和溴乙烷:分液 | D. | 分离氯化钠和硝酸钾:结晶 |
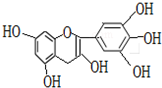 茶是我国的传统饮品,茶叶中含有的茶多酚可以替代食品添加剂中对人体有害的合成抗氧化剂,用于多种食品保鲜等,如图1所示是茶多酚中含量最高的一种儿茶素A的结构简式,关于这种儿茶素A的有关叙述正确的是( )
茶是我国的传统饮品,茶叶中含有的茶多酚可以替代食品添加剂中对人体有害的合成抗氧化剂,用于多种食品保鲜等,如图1所示是茶多酚中含量最高的一种儿茶素A的结构简式,关于这种儿茶素A的有关叙述正确的是( )