题目内容
在2NO+O2?2NO2(正反应为吸热反应)中,下列表明在30℃和100℃时平衡体系中,NO的百分含量与压强(p)或压强一定时与时间的关系图象,正确的是( )
A、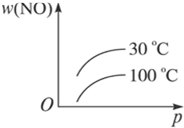 |
B、 |
C、 |
D、 |
考点:产物的百分含量随浓度、时间的变化曲线
专题:化学平衡专题
分析:根据影响化学反应速率和化学平衡的因素进行判断得出正确结论.升高温度,化学反应速率加快,平衡向着吸热的方向移动;增大压强,化学反应速率加快,平衡向着气体体积减小的方向移动.
解答:
解:2NO+O2?2NO2(正反应为吸热反应)
A.升高温度,平衡正向移动,NO的百分含量减小,与图象不符,故A错误;
B.升高温度,化学反应速率加快,达到平衡的时间缩短,与图象不符,故B错误;
C.升高温度,平衡正向移动,NO的百分含量减小,与图象不符,故C错误;
D.升高温度,平衡正向移动,NO的百分含量减小;增大压强,平衡正向移动,NO的百分含量减小;与图象相符,故D正确;
故选D.
A.升高温度,平衡正向移动,NO的百分含量减小,与图象不符,故A错误;
B.升高温度,化学反应速率加快,达到平衡的时间缩短,与图象不符,故B错误;
C.升高温度,平衡正向移动,NO的百分含量减小,与图象不符,故C错误;
D.升高温度,平衡正向移动,NO的百分含量减小;增大压强,平衡正向移动,NO的百分含量减小;与图象相符,故D正确;
故选D.
点评:本题结合图象考查外界条件对化学反应速率和化学平衡的影响,难度中等.

练习册系列答案
相关题目
某结晶水合物的分子式为R?nH2O其相对分子质量为M,在25℃时,ag该晶体溶于bg水中,即达到饱和,形成V mL密度为dg/cm3的溶液.下列表达式中正确的是( )
A、该饱和溶液的物质的量浓度为
| ||
B、25℃时,R的溶解度为
| ||
C、该饱和溶液的物质的量浓度为
| ||
D、该饱和溶液的质量分数为
|
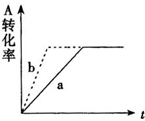 已知某可逆反应在密闭容器中进行.A(g)+2B(g)?C(g)+D(s)放出热量,图中曲线a代表一定条件下该反应的过程.若使a曲线变为b曲线,可采取的措施是( )
已知某可逆反应在密闭容器中进行.A(g)+2B(g)?C(g)+D(s)放出热量,图中曲线a代表一定条件下该反应的过程.若使a曲线变为b曲线,可采取的措施是( )| A、增大A的浓度 |
| B、缩小容器的容积 |
| C、加入催化剂 |
| D、升高温度 |
某物质灼烧时,焰色反应为黄色,则下列判断不正确的是( )
| A、该物质可能是钠的化合物 |
| B、该物质一定含钠元素 |
| C、该物质一定是金属钠 |
| D、不能确定该物质中是否含有钾元素 |
下列药品若用氯气消毒过的自来水来配制,会变质的是( )
| A、Na2SO4 |
| B、NaCl |
| C、AgNO3 |
| D、K2CO3 |
下列关于金属腐蚀的说法中,正确的是( )
| A、金属腐蚀的实质是金属原子失去电子被还原的过程 |
| B、金属的化学腐蚀必须在酸性条件下进行 |
| C、化学腐蚀比电化学腐蚀要普遍的多 |
| D、在轮船船身上装上一定数量的锌块可以防止钢铁的腐蚀 |
下列各组离子能大量共存的是( )
| A、Na+ NH4+ S2- AlO2- |
| B、Fe3+ K+ HSO3- Cl- |
| C、NH4+ Ca2+ HCO3-AlO2- |
| D、Fe2+ Mg2+ SO42- NO3- |
以下实验基本操作正确的是( )
A、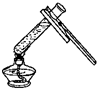 加热液体 |
B、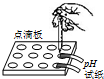 测定溶液pH |
C、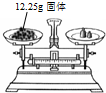 称量固体 |
D、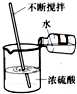 稀释浓硫酸 |
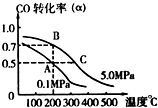 在10L密闭容器中充有10mol CO 与20mol H2,在催化剂作用下反应生成甲醇:
在10L密闭容器中充有10mol CO 与20mol H2,在催化剂作用下反应生成甲醇: