题目内容
将一定量的氧化铜粉末加入到100mL 0.5mol/L的硫酸溶液中微热至氧化铜全部溶解,再向该蓝色溶液中加入足量的铁粉,充分反映后,收集到H2在标准状态下的体积为0.224L,求:
(1)参加反应的铁的质量;
(2)原加入氧化铜的质量为多少克?
(3)如果最后所得溶液100L,其所得溶液的物质的量浓度是多少?
(1)参加反应的铁的质量;
(2)原加入氧化铜的质量为多少克?
(3)如果最后所得溶液100L,其所得溶液的物质的量浓度是多少?
考点:化学方程式的有关计算
专题:
分析:常温下,将氧化铜加入到溶液中,发生反应CuO+H2SO4=CuSO4+H2O,再向溶液中加入足量铁粉,充分反应,此时收集到气体为0.224L(标准状况)的氢气,说明硫酸有剩余,加入的铁发生反应Fe+Cu2+=Cu+Fe2+、Fe+2H+=Fe2++H2↑,置换出溶液中的铜、与氢气,据此分别计算即可.
解答:
解:常温下,将氧化铜加入到溶液中,发生反应CuO+H2SO4=CuSO4+H2O,再向溶液中加入足量铁粉,充分反应,此时收集到气体为0.224L(标准状况)的氢气,说明硫酸有剩余,加入的铁发生反应Fe+Cu2+=Cu+Fe2+、Fe+2H+=Fe2++H2↑,置换出溶液中的铜、与氢气.
(1)加入足量铁粉后的溶液中溶质是硫酸亚铁,根据硫酸根守恒n(H2SO4)=n(FeSO4)=0.05mol=n(Fe),所以参加反应的铁的质量为:0.05mol×56g/mol=2.8g,答:参加反应的铁的质量为2.8g;
(2)依据氧化还原反应得失电子守恒有:氢气得到电子数:
×2=0.02mol;Fe失去的总电子数为:0.05mol×2=0.1mol,故铜得到的电子数为:0.1mol-0.02mol=0.08mol,即加入氧化铜的质量为:0.04mol×80g/mol=3.2g;答:原加入氧化铜的质量为3.2克.
(3)最后所得溶液100mL,为FeSO4,其物质的量浓度是:
=0.5mol/L,
答:最后所得硫酸亚铁的物质的量浓度是0.5mol/L.
(1)加入足量铁粉后的溶液中溶质是硫酸亚铁,根据硫酸根守恒n(H2SO4)=n(FeSO4)=0.05mol=n(Fe),所以参加反应的铁的质量为:0.05mol×56g/mol=2.8g,答:参加反应的铁的质量为2.8g;
(2)依据氧化还原反应得失电子守恒有:氢气得到电子数:
| 0.224L |
| 22.4L/mol |
(3)最后所得溶液100mL,为FeSO4,其物质的量浓度是:
| 0.05mol |
| 0.1L |
答:最后所得硫酸亚铁的物质的量浓度是0.5mol/L.
点评:本题考查化学方程式的计算,侧重于学生的分析能力和计算能力的考查,属于常考题.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
甲、乙、丙、丁4中物质分别含2种或3种元素,它们的分子中各含18个电子.甲是气态氢化物,在水中分步电离出两种阴离子.下列推断合理的是( )
| A、某钠盐溶液含甲电离出的阴离子,则该溶液显碱性,只能与酸反应 |
| B、乙与氧气的摩尔质量相同,则乙属于分子晶体,其沸点一定和氧气相近 |
| C、丙中含有第二周期IVA族的元素,则丙一定是甲烷的同系物 |
| D、丁和甲中各元素质量比相同,则1mol 丁分子含有3NA个共用电子对 |
有一瓶Na2SO3溶液,由于它可能部分被氧化,某同学进行如下实验:取少量溶液,滴入Ba(NO3)2溶液,有白色沉淀产生,再加入足量稀HNO3,充分振荡后,仍有白色沉淀.对此下述结论正确的是( )
| A、Na2SO3已部分氧化 |
| B、加入Ba(NO3)2溶液所生成的沉淀一定含有BaSO4 |
| C、加入HNO3后的沉淀一定是BaSO4 |
| D、此实验不能确定Na2SO3是否被氧化 |
甲烷燃烧的化学方程式为CH4+2O2=CO2+2H2O.常温常压下,将1体积甲烷在3体积氧气中完全燃烧,再将生成的气体恢复到原来的温度和压强.求生成多少体积的二氧化碳?剩余什么气体?它的体积是多少??
下表所列各组物质中,物质之间按箭头方向通过一步反应不能实现如图所示转化的是( )
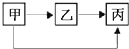

| 物质 选项 | 甲 | 乙 | 丙 |
| A | CuO | CO2 | H2O |
| B | C | CO | CO2 |
| C | CaCO3 | CaO | Ca(OH)2 |
| D | H2SO4 | H2O | H2 |
| A、A | B、B | C、C | D、D |
在常温下,PH=a的醋酸和PH=14-a的NaOH溶液等体积混合,所得溶液的下列说法正确的是( )
| A、PH<7 |
| B、PH=7 |
| C、PH>7 |
| D、上述三种均有可能 |