题目内容
常温下,下列各组离子在指定溶液中可能大量共存的是( )
| A、1 mol?L-1NaHCO3溶液中:Ca2+、Fe3+、NO3-、Cl- |
| B、pH=1的溶液中:K+、Mg2+、SO32-、NO3- |
| C、由水电离出的c(H+)=1.0×10-13 mol?L-1溶液中:Mg2+、Na+、SO42-、Br- |
| D、c(NH3?H2O)=1 mol?L-1的溶液中:NH4+、Al3+、SO42-、Cl- |
考点:离子共存问题
专题:离子反应专题
分析:离子之间生成气体、沉淀、弱电解质、络合物或发生氧化还原反应、双水解反应的就不能共存,
A.碳酸根离子和铁离子发生双水解;
B.pH=1的溶液呈强酸性,弱酸根离子不能大量共存;
C.由水电离出的c(H+)=1.0×10-13 mol?L-1溶液呈酸性或碱性,则和氢离子或氢氧根离子反应的离子不能共存;
D.氨水溶液呈碱性,则和氢氧根离子反应的离子不能大量共存.
A.碳酸根离子和铁离子发生双水解;
B.pH=1的溶液呈强酸性,弱酸根离子不能大量共存;
C.由水电离出的c(H+)=1.0×10-13 mol?L-1溶液呈酸性或碱性,则和氢离子或氢氧根离子反应的离子不能共存;
D.氨水溶液呈碱性,则和氢氧根离子反应的离子不能大量共存.
解答:
解:离子之间生成气体、沉淀、弱电解质、络合物或发生氧化还原反应、双水解反应的就不能共存,
A.HCO3-和Fe3+发生双水解反应生成Fe(OH)3和CO2而不能大量共存,故A错误;
B.pH=1的溶液呈强酸性,弱酸根离子SO32-不能大量共存,故B错误;
C.由水电离出的c(H+)=1.0×10-13 mol?L-1溶液呈酸性或碱性,则和Mg2+和氢氧根离子反应的离子不能共存,但酸性条件下,这离子离子不反应且和氢离子也不反应,所以能大量共存,故C正确;
D.氨水溶液呈碱性,则Al3+和氢氧根离子反应生成氢氧化铝而不能大量共存,故D错误;
故选C.
A.HCO3-和Fe3+发生双水解反应生成Fe(OH)3和CO2而不能大量共存,故A错误;
B.pH=1的溶液呈强酸性,弱酸根离子SO32-不能大量共存,故B错误;
C.由水电离出的c(H+)=1.0×10-13 mol?L-1溶液呈酸性或碱性,则和Mg2+和氢氧根离子反应的离子不能共存,但酸性条件下,这离子离子不反应且和氢离子也不反应,所以能大量共存,故C正确;
D.氨水溶液呈碱性,则Al3+和氢氧根离子反应生成氢氧化铝而不能大量共存,故D错误;
故选C.
点评:本题考查离子共存,为考试热点,明确离子共存条件及离子性质是解本题关键,易错选项是C,注意该溶液可能是酸性或碱性,为易错点.

练习册系列答案
相关题目
下列物质与其用途完全符合的有几条( )
①Na2CO3-制玻璃②SiO2-太阳能电池③AgI-人工降雨④NaCl-制纯碱⑤Al2O3-焊接钢轨⑥NaClO-消毒剂
⑦MgO-耐火材料⑧Fe2O3-红色油漆或涂料.
①Na2CO3-制玻璃②SiO2-太阳能电池③AgI-人工降雨④NaCl-制纯碱⑤Al2O3-焊接钢轨⑥NaClO-消毒剂
⑦MgO-耐火材料⑧Fe2O3-红色油漆或涂料.
| A、4 | B、5 | C、6 | D、7 |
下列物质中,不能用做抗酸药的是( )
| A、氢氧化铝 | B、碳酸钡 |
| C、碳酸氢钠 | D、碳酸镁 |
在无色透明的强酸性溶液中,能大量共存的是( )
| A、Ca2+、K+、HCO3-、Na+ |
| B、Fe3+、Cl-、H+、NO3- |
| C、Mg2+、Na+、NO3-、Cl- |
| D、K+、OH-、Cl-、SO42- |
下列叙述中,不正确的是( )
| A、氯水中的次氯酸具有杀菌消毒作用 |
| B、陶瓷的主要成分是碳酸钙 |
| C、硅是制造太阳能电池的常用材料 |
| D、漂白粉的有效成分是次氯酸钙 |
如图所示,将铁棒和石墨棒插入盛有饱和NaCl溶液的U型管中,下列分析正确的是( )
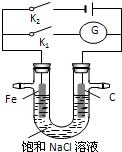

| A、K1闭合,铁棒上发生的反应为2H++2e-→H2↑ |
| B、K1闭合,石墨棒周围溶液pH逐渐升高 |
| C、K2闭合,铁棒不会被腐蚀,属于牺牲阳极的阴极保护法 |
| D、K2闭合,电路中通过0.4NA个电子时,两极共产生标况下4.48L气体 |