题目内容
14.用双线桥标出下列反应中的电子转移的方向及数目,并指出氧化剂和还原剂(1)3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O,氧化剂是HNO3,还原剂为Cu,氧化产物是Cu(NO3)2;
(2)2FeCl3+2HI═2FeCl2+2HCl+I2,氧化剂是FeCl3,还原产物是FeCl2,还原剂为HI.
分析 (1)Cu元素的化合价升高,N元素的化合价降低,转移6e-;
(2)Fe元素的化合价降低,I元素的化合价升高,该反应转移2e-,以此来解答.
解答 解:(1)该反应中Cu元素化合价由0价变为+2价、Cu为还原剂,被氧化,对应氧化产物为,部分N元素化合价由+5价变为+2价,则HNO3为氧化剂,其得失电子最小公倍数是6,用双线桥标出该反应电子转移的方向和数目为 ,
,
故答案为: ;HNO3;Cu;Cu(NO3)2;
;HNO3;Cu;Cu(NO3)2;
(2)Fe元素化合价从+3价变化为+2价得到电子,则FeCl3为氧化剂,对应还原产物为FeCl2;碘元素化合价从-1价变化为0价,则HI为还原剂,用双线桥标注电子转移为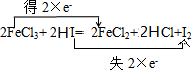 ,
,
故答案为: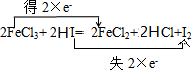 ;FeCl3;FeCl2;HI.
;FeCl3;FeCl2;HI.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念及转移电子表示方法的考查,题目难度不大.

练习册系列答案
相关题目
4.近年来,多地公共汽车大部分采用天然气或燃料电池作为动力,其主要目的是( )
| A. | 减少对大气的污染 | B. | 降低成本 | ||
| C. | 防止石油短缺 | D. | 加大发动机的动力 |
5.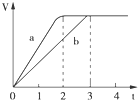 镁粉和铝粉分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系如图,下列说法正确的是( )
镁粉和铝粉分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系如图,下列说法正确的是( )
 镁粉和铝粉分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系如图,下列说法正确的是( )
镁粉和铝粉分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系如图,下列说法正确的是( )| A. | 镁粉和铝粉的物质的量之比为3:2 | |
| B. | 镁粉和铝粉质量之比为3:2 | |
| C. | 镁粉和铝粉的摩尔质量之比为2:3 | |
| D. | 镁粉和铝粉反应完所需时间之比为3:2 |
6.下列叙述中不正确的是( )
| A. | Na2O2是淡黄色固体,Na2O 是白色固体,二者都能与水反应生成 NaOH | |
| B. | Na和O2在加热时反应生成 Na2O2,在常温下反应生成 Na2O | |
| C. | Na2O与CO2发生化合反应生成Na2CO3,Na2O2与CO2发生置换反应生成 O2 | |
| D. | 2 g H2充分燃烧后产物被Na2O2完全吸收,Na2O2固体增重2g |
3.下列关于NH3性质的说法正确的是( )
| A. | 收集时采用向上排空气法 | B. | 能使湿润的红色石蕊试纸变蓝 | ||
| C. | 可用浓硫酸进行干燥 | D. | 不能与氧气反应 |
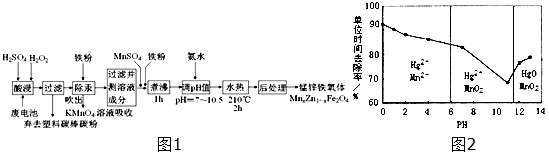
 ;
;
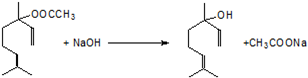 ,.
,.