题目内容
混合物由金属M的盐酸盐和其氧化合,以及另一种金 属N的氧化物组成。有以下反应关系:
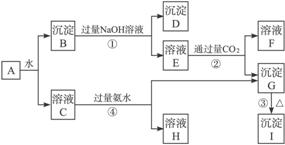
据此判断:
(1)沉淀D的化学式为___________________________________。
(2)反应③的化学方程式为________________________________。
(3)反应①②④的离子方程式为
①__________________________________________________,②___________________________________,④____________________________________。
(1)Fe2O3
(2)2Al(OH)3![]() Al2O3+3H2O
Al2O3+3H2O
(3)①Al2O3+2OH-====2![]() +H2O
+H2O
②OH-+CO2=![]()
![]() +2H2O+CO2====
+2H2O+CO2====![]() +Al(OH)3↓
+Al(OH)3↓
④Al3++3NH3·H2O====Al(OH)3↓+3![]()
解析:
由A中各物质的性质可推知B中含Al2O3和Fe2O3,C中溶质为KAl(SO4)2。反应④为Al3+与NH3·H2O生成Al(OH)3,故G为Al(OH)3。B中Al2O3与NaOH反应,故D为Fe2O3,E中含![]() 和过量的OH-。由此推知,
和过量的OH-。由此推知,![]() 与CO2反应生成Al(OH)3,这是由于Al(OH)3比H2CO3酸性弱的缘故,同时由于CO2过量,反应②应生成
与CO2反应生成Al(OH)3,这是由于Al(OH)3比H2CO3酸性弱的缘故,同时由于CO2过量,反应②应生成![]() 。反应③为Al(OH)3受热分解生成Al2O3和H2O。
。反应③为Al(OH)3受热分解生成Al2O3和H2O。

 阶梯计算系列答案
阶梯计算系列答案(14分)不同的金属在化学反应中表现出来的活泼程度不同,瑞典化学家贝采里乌斯和俄国化学家贝开托夫称之为金属活动顺序。另一方面,同一金属在不同条件或不同化学反应中也可以表现出不同的活泼程度。
⑴根据金属活动性顺序,工业上冶炼金属可以采用不同的冶炼方法。其中可以用“热分解法”冶炼的金属有 。
腐蚀速率/g.m-2.h-1
 ⑵工业上用氯化铁溶液腐蚀铜制电路板。根据金属活动性顺序及该反应原理,比较Cu2+、Fe3+、Fe2+的氧化性由强到弱的顺序: 。
⑵工业上用氯化铁溶液腐蚀铜制电路板。根据金属活动性顺序及该反应原理,比较Cu2+、Fe3+、Fe2+的氧化性由强到弱的顺序: 。
⑶合金Fe-Cr在不同酸中反应情况不同,其在三种稀硫
酸、稀硝酸和稀盐酸中的腐蚀速率如图所示,则下列
有关说法正确的是 (填写序号)。
A.酸的氧化性越强,对该合金的腐蚀速率越大
B.稀硝酸对该合金的腐蚀性比另两种酸弱
C.合金中Cr含量增加,稀硝酸对该合金的腐蚀性减弱
⑷已知粗铜中含有少量的锌、铁、银、金等金属和少量
|
以硫酸铜溶液为电解液,用电解的方法实现了粗铜的提纯,
并对阳极泥和电解液中金属进行回收。
步骤一:电解精制
电解时,粗铜应与电源的 极相连。电解过程中,硫酸铜的浓度会 (填“变大”、“不变”或“变小”)。
步骤二:电解完成后,该小组同学按以下流程对电解液进行处理:

稀硝酸处理阳极泥得到硝酸银稀溶液,请你写出该步反应的离子方程式: 。
残渣含有极少量的黄金,如何回收金,他们查阅了有关资料,了解到了一些有关金的知识,以下是他们获取的一些信息:
| 序号 | 反应 | 平衡常数 |
| 1 | Au + 6HNO3(浓)= Au(NO3)3 + 3NO2↑+ 3H2O | << 1 |
| 2 | Au3+ + 4Cl- = AuCl4- | >>1 |
从表中可知,金很难与硝酸反应,但却可溶于王水(浓硝酸与盐酸按体积比1:3的混合物),请你简要解释金能够溶于王水的原因: 。


