题目内容
现有反应aA(g)+bB(g)?pC(g),达到平衡后,当升高温度时,B的转化率变大:当减小压强时,混合体系中C的质量分数减小,则:
(1)该反应的正反应是 热反应;且a+b p(填“>”“<”’或“=”).
(2)减压时,正反应速率 (填“增大”“减小”或“不变”).
(3)若加入催化剂,平衡时气体混合物的总物质的量 .(填“增大”“减小”或“不变”).
(4)若B是有色物质,A、C均为无色物质,则加入C(体积不变)时混合物的颜色 ,而维持容器内气体的压强不变,充入氖气时,混合物的颜色 .(填“变浅”“变深”或“不变”)
(1)该反应的正反应是
(2)减压时,正反应速率
(3)若加入催化剂,平衡时气体混合物的总物质的量
(4)若B是有色物质,A、C均为无色物质,则加入C(体积不变)时混合物的颜色
考点:化学平衡的影响因素,反应热和焓变
专题:化学平衡专题
分析:达到平衡后,当升高温度时,B的转化率变大,说明温度升高平衡向正反应方向移动,则正反应吸热;
当减小压强时,混合体系中C的质量分数也减小,说明压强减小平衡向逆反应方向移动,则方程式中反应物的气体的计量数之和大于生成物气体的化学计量数之和;催化剂不影响平衡移动,根据外界条件对化学平衡的影响解答该题.
当减小压强时,混合体系中C的质量分数也减小,说明压强减小平衡向逆反应方向移动,则方程式中反应物的气体的计量数之和大于生成物气体的化学计量数之和;催化剂不影响平衡移动,根据外界条件对化学平衡的影响解答该题.
解答:
解:(1)达到平衡后,当升高温度时,B的转化率变大,说明温度升高平衡向正反应方向移动,则正反应吸热,逆反应为放热反应,当减小压强时,混合体系中C的质量分数也减小,说明压强减小平衡向逆反应方向移动,则方程式中反应物的气体的计量数之和大于生成物气体的化学计量数之和;
故答案为:吸;>;
(2)减压时正逆反应速率都减小,正反应反应速率减小,故答案为:减小;
(3)催化剂只能加快化学反应速率,不影响平衡移动,故答案为:不变;
(4)加入A(体积不变)时,化学平衡正向移动,所以混合物颜色加深,保持容器压强不变,充入氖气时,各组分浓度减小,所以混合物颜色变浅,故答案为:变深;变浅.
故答案为:吸;>;
(2)减压时正逆反应速率都减小,正反应反应速率减小,故答案为:减小;
(3)催化剂只能加快化学反应速率,不影响平衡移动,故答案为:不变;
(4)加入A(体积不变)时,化学平衡正向移动,所以混合物颜色加深,保持容器压强不变,充入氖气时,各组分浓度减小,所以混合物颜色变浅,故答案为:变深;变浅.
点评:本题考查外界条件对平衡移动的影响,注意催化剂不影响平衡移动,题目难度不大.

练习册系列答案
 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案
相关题目
如图是配制一定物质的量浓度溶液的过程示意图.下列说法中错误的是( )
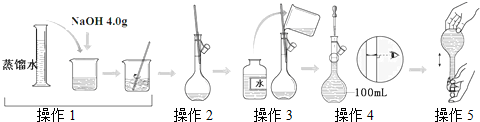

| A、所配制的NaOH溶液物质的量浓度为1.0 mol/L |
| B、操作2是将NaOH加水溶解后直接转移到容量瓶中 |
| C、操作4是滴加水至溶液凹液面的最低点与刻度线平齐 |
| D、操作5中,定容摇匀后发现液面低于刻度线,不能再继续加水 |
 向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:xA(g)+B(g)?2C(g).各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别用下表和如图表示:下列说法正确的是( )
向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:xA(g)+B(g)?2C(g).各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别用下表和如图表示:下列说法正确的是( )| 容器 | 甲 | 乙 | 丙 |
| 容积 | 0.5L | 0.5L | 1.0L |
| 温度 | T1 | T2 | T2 |
| 反应物 起始量 | 0.5molA 1.5molB | 0.5molA 1.5molB | 2.0molA 6.0molB |
| A、由图可知:T1<T2,且该反应为吸热反应 |
| B、T2时该反应的平衡常数K=0.8 |
| C、前10min乙、丙两容器中v(A)乙>v(A)丙 |
| D、C的质量m:m甲=m乙<2m丙 |
室温下,等体积的、pH=2的 HCl和CH3COOH溶液,以下说法正确的是( )
| A、两溶液中由水电离的c(H+)前者小于后者 |
| B、两溶液分别和足量的锌反应,生成氢气的体积相等 |
| C、两溶液分别和相同的锌反应,生成氢气的起始速率相等 |
| D、两溶液分别和与其体积相等的、pH=12的NaOH溶液混合后,都呈中性 |
下列实验操作正确的是( )
| A、将氢氧化钠固体放在滤纸上称量 |
| B、用10 mL量筒量取8.58 mL蒸馏水 |
| C、硅酸钠溶液保存在橡胶塞的试剂瓶中 |
| D、用广泛pH试纸测定某浓度醋酸溶液的pH为4.5 |
下列行为符合实验安全要求的是( )
| A、实验室废液可直接排入下水道 |
| B、制备有毒气体应在通风橱内进行 |
| C、配制稀硫酸时将水倒入浓硫酸中并不断搅拌 |
| D、不慎洒出的酒精在桌上着火时,立即用大量水扑灭 |
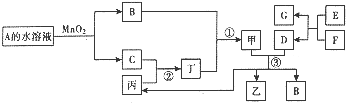 已知化合物A与B、丙与丁的组成元素相同,且四种物质中都含有同一种元素.A与B在常温下呈液态.D与F为常见金属单质,且D、F分别与甲的浓溶液分别在常温作用都无明显现象,加热时都有大量气体产生.E是一种红棕色粉末,A与丙可化合生成甲,乙、丙和B在常温下也可以生成甲和另一种化合物X,其部分转化关系如图(相关转化中部分反应条件和生成物未标出).
已知化合物A与B、丙与丁的组成元素相同,且四种物质中都含有同一种元素.A与B在常温下呈液态.D与F为常见金属单质,且D、F分别与甲的浓溶液分别在常温作用都无明显现象,加热时都有大量气体产生.E是一种红棕色粉末,A与丙可化合生成甲,乙、丙和B在常温下也可以生成甲和另一种化合物X,其部分转化关系如图(相关转化中部分反应条件和生成物未标出).