题目内容
4.用下列物质的编号填空:①NaCl晶体 ②盐酸 ③HCl ④熔融KCl ⑤蔗糖 ⑥铜 ⑦CO2 ⑧稀硫酸 ⑨KOH溶液;
以上物质中属于电解质的是①③④,属于非电解质的是⑤⑦,能导电的是②④⑥⑧⑨.
分析 在水溶液里或熔融状态下能导电的化合物是电解质;在水溶液里和熔融状态下都不导电的化合物是非电解质;含有自由移动离子或电子的物质能导电;
解答 解:氯化钠晶体、HCl、熔化的KCl溶于水或熔融状态下都能电离出阴阳离子,所以其水溶液或熔融状态都能导电,为电解质,故选①③④;
CO2的水溶液能导电,但电离出阴阳离子的物质是碳酸而不是二氧化碳,蔗糖在水溶液里以分子存在,所以氨气和酒精都是非电解质,故选⑤⑦;
盐酸、熔化KCl、稀硫酸、KOH溶液中含有自由移动的离子,铜中含有自由移动的电子,所以铜、盐酸、熔化KCl、稀硫酸、KOH溶液导电,故选②④⑥⑧⑨;
故答案为:①③④;⑤⑦;②④⑥⑧⑨.
点评 本题考查了非电解质和电解质的判断,根据概念来分析解答即可,注意电解质不一定导电,导电的不一定是电解质,为易错点,题目难度不大.

练习册系列答案
 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案
相关题目
9.某学生用量筒量取液体,量筒放平稳后仰视液面读得数值为 19mL,倾倒部分液体后,又俯视液面,读得数值为10mL. 则该学生实际倾倒的液体体积是( )
| A. | 9mL | B. | 小于9mL | ||
| C. | 大于9 mL | D. | 因操作错误无法判断 |
13. 用中和滴定法测定某盐酸的物质的量浓度.
用中和滴定法测定某盐酸的物质的量浓度.
(1)标准溶液应盛于A(填“A”或“B”)滴定管中.
(2)若选用酚酞作指示剂,以0.125 0mol•L-1的标准氢氧化钠溶液滴定,如何判断滴定终点当加入最后一滴标准液时,溶液恰好出现红色且半分钟内红色不褪去
(3)实验数据记录如表,请分析数据并计算,盐酸的物质的量浓度=0.1250mol•L-1
 用中和滴定法测定某盐酸的物质的量浓度.
用中和滴定法测定某盐酸的物质的量浓度.(1)标准溶液应盛于A(填“A”或“B”)滴定管中.
(2)若选用酚酞作指示剂,以0.125 0mol•L-1的标准氢氧化钠溶液滴定,如何判断滴定终点当加入最后一滴标准液时,溶液恰好出现红色且半分钟内红色不褪去
(3)实验数据记录如表,请分析数据并计算,盐酸的物质的量浓度=0.1250mol•L-1
| 滴定次数 | 待测液体体积/mL | 标准碱液 | |
| 滴定前读数/mL | 滴定后读数/mL | ||
| ① | 20.0 | 0.40 | 20.41 |
| ② | 20.0 | 0.10 | 20.60 |
| ③ | 20.0 | 4.00 | 23.99 |
14.设NA为阿伏加德罗常数,下列说法中正确的是( )
| A. | NA个氢气分子所占的体积为22.4L | B. | 2NA个二氧化碳分子的质量为44g | ||
| C. | 32g O2所含的氧原子数目是2NA | D. | 17g氨气中所含原子数为NA |
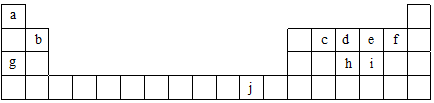
 .
. ,ci2与ce2比较,沸点较高的是CS2(写分子式).
,ci2与ce2比较,沸点较高的是CS2(写分子式). .
.