题目内容
根据杂化轨道理论,指出下列分子中心原子采取的杂化轨道类型及空间构型.
分子 杂化轨道类型 空间构型
①CH4 、 ;
②C2H4 、 ;
③C2H2 、 ,其中σ键与π键数之比为 .
分子 杂化轨道类型 空间构型
①CH4
②C2H4
③C2H2
考点:原子轨道杂化方式及杂化类型判断
专题:化学键与晶体结构
分析:根据价层电子对互斥理论确定分子的空间构型及原子杂化方式,价层电子对个数=σ键个数+孤电子对个数,据此分析解答.
解答:
解:①CH4中价层电子对个数=4+
×(4-4×1)=4且不含孤电子对,所以C原子采用sp3杂化,其空间构型为正四面体结构,故答案为:sp3;正四面体;
②C2H4中每个碳原子价层电子对个数为3且不含孤电子对,所以C原子采用sp2杂化,且平面结构,故答案为:sp2;平面形;
③乙炔的结构式为H-C≡C-H,每个碳原子价层电子对个数是2且不含孤电子对,所以C原子采用sp杂化,为直线形结构,该反应中σ键与π键个数=3:2,故答案为:sp;直线形;3:2.
| 1 |
| 2 |
②C2H4中每个碳原子价层电子对个数为3且不含孤电子对,所以C原子采用sp2杂化,且平面结构,故答案为:sp2;平面形;
③乙炔的结构式为H-C≡C-H,每个碳原子价层电子对个数是2且不含孤电子对,所以C原子采用sp杂化,为直线形结构,该反应中σ键与π键个数=3:2,故答案为:sp;直线形;3:2.
点评:本题考查了原子杂化方式的判断,根据价层电子对互斥理论解答即可,注意孤电子对个数的计算方法,知道其表达式中各个字母的含义,题目难度不大.

练习册系列答案
 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案
相关题目
下列说法错误的( )
| A、分别充满HCl、NH3的烧瓶倒置于水中后液面迅速上升,说明二者均易溶于水 | ||||||
B、向NH4HCO3溶液中加过量的NaOH溶液并加热,离子方程式为:NH
| ||||||
| C、用NH4Cl固体和Ca(OH)2固体制备并收集NH3,需要的玻璃仪器有酒精灯、大试管、导管、集气瓶 | ||||||
| D、用湿润的红色石蕊试纸检验氨气 |
NA表示阿伏加德罗常数的值,4℃时,25滴水为amL,则1滴水中含有的水分子数为( )
| A、aNA/25 |
| B、aNA/(25×18) |
| C、aNA/(25×20) |
| D、aNA/(1000×22.4) |
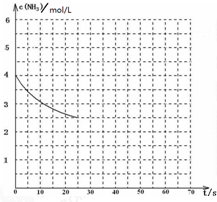 氨是最重要的化工产品之一.
氨是最重要的化工产品之一.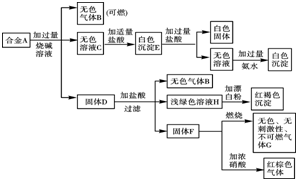 现有四种单质组成的合金A,为分析其成分,用此合金进行一系列实验,其过程及发生反应的现象如下图所示.
现有四种单质组成的合金A,为分析其成分,用此合金进行一系列实验,其过程及发生反应的现象如下图所示.