题目内容
下列离子方程式书写正确的是( )
| A、向CuSO4溶液中加入钠:Na+Cu2+=Cu+Na+ |
| B、向Ba(OH)2溶液中滴加稀盐酸:2H++2Cl-+Ba2++2OH-=2H2O+BaCl2 |
| C、澄清石灰水与盐酸反应:H++OH-=H2O |
| D、往FeCl3溶液中加入Cu粉:2Fe3++3Cu=2Fe+3Cu2+ |
考点:离子方程式的书写
专题:离子反应专题
分析:A.不符合反应的客观事实,钠与硫酸铜溶液反应生成氢氧化铜沉淀、氢气和硫酸钠;
B.氯化钡为可溶性盐,应拆成离子形式;
C.氢氧化钙溶液与盐酸反应生成氯化钙和水;
D.不符合反应的客观事实,FeCl3溶液中加入Cu粉发生氧化还原反应生成氯化亚铁、氯化铜.
B.氯化钡为可溶性盐,应拆成离子形式;
C.氢氧化钙溶液与盐酸反应生成氯化钙和水;
D.不符合反应的客观事实,FeCl3溶液中加入Cu粉发生氧化还原反应生成氯化亚铁、氯化铜.
解答:
解:A.向CuSO4溶液中加入钠,反应的离子方程式:2H2O+2Na+Cu2+=Cu(OH)2↓+2Na++H2↑,故A错误;
B.向Ba(OH)2溶液中滴加稀盐酸,离子方程式为:H++OH-=H2O,故B错误;
C.澄清石灰水与盐酸反应,离子方程式:H++OH-=H2O,故C正确;
D.往FeCl3溶液中加入Cu粉,离子方程式:2Fe3++Cu=2Fe2++Cu2+,故D错误;
故选:C.
B.向Ba(OH)2溶液中滴加稀盐酸,离子方程式为:H++OH-=H2O,故B错误;
C.澄清石灰水与盐酸反应,离子方程式:H++OH-=H2O,故C正确;
D.往FeCl3溶液中加入Cu粉,离子方程式:2Fe3++Cu=2Fe2++Cu2+,故D错误;
故选:C.
点评:本题考查了离子方程式的书写,明确反应的实质是解题关键,注意离子方程式书写应符合客观规律、遵循电荷守恒、原子个数守恒,题目难度不大.

练习册系列答案
相关题目
根据对角线原则,Be和Al的化学性质相似,下列说法正确是( )
| A、BeCl2溶液 pH>7,将其蒸干,灼烧后可得到BeCl2晶体 |
| B、BeCl2溶液能导电,说明BeCl2一定是离子化合物 |
| C、Be(OH)2既能溶于盐酸,又能溶于NaOH溶液 |
| D、Be只能与盐酸反应,不能与NaOH溶液反应 |
阿伏加德罗常数约为6.02×1023mol-1,下列叙述中正确的是( )
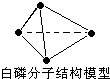

| A、31g 白磷分子(P4)中含有P-P键个数为1.5×6.02×1023 |
| B、48gO2和48gO3所含分子数为3×6.02×1023 |
| C、1.0L 1mol/L氨水中,NH3?H2O的分子数为6.02×1023 |
| D、20g 重水(D2O)中含有的中子数为8×6.02×1023 |
常温下,下列各组离子在指定溶液中可能大量共存的是( )
| A、0.l mol?L-1的NaAlO2溶液:K+、Na+、SO42-、CO32- |
| B、使pH试纸变蓝的溶液中:NH4+、Na+、SO42-、Cl- |
| C、含有大量ClO-溶液中:K+、OH-、I-、SO32- |
| D、c(Al3+)=0.1 mol?L-1的溶液中:Na+、Cl-、AlO2-、SO42- |
下列关于氢氧化铁胶体的叙述,正确的是( )
| A、往氢氧化铁胶体中逐滴加入稀盐酸先出现沉淀后沉淀溶解 |
| B、在含2 mol的氢氧化铁的胶体中含有氢氧化铁胶粒数为2NA |
| C、滤纸可将氢氧化铁胶体中的分散质与分散剂分离 |
| D、氢氧化铁胶体带正电荷 |
下列物质按一定的分类方法,属于同一类的是( )
| A、标准状况下的状态:O2、CO2、H2O |
| B、酸性氧化物:SO2、Cl2O7、N2O5 |
| C、碱性氧化物:Na2O、CaO、Al2O3 |
| D、混合物:漂白粉、氯水、液氯 |
分类法是一种行之有效、简单易行的科学方法,人们在认识事物时可以采取多种分类方法,下列关于“NaHCO3”的分类错误的是( )
| A、酸式盐 | B、可溶盐 | C、钠盐 | D、酸 |
欲除去铁粉中混有的少量铝粉,应选用的试剂是( )
| A、稀盐酸 | B、稀硝酸 |
| C、硫酸铜溶液 | D、氢氧化钠溶液 |
目前,安全生产和食品、药品安全受到人们的高度重视.下列有关说法不正确的是( )
| A、检查病人胃病所用的钡餐,只能用BaSO4,不可以用BaCO3 |
| B、为了使馒头、银耳等洁白、卖相好,可以用硫黄熏蒸它们 |
| C、可以用SO2来漂白纸浆、毛、丝、草帽辫等 |
| D、氯气溶于水生成次氯酸可以用于自来水的消毒 |