题目内容
12.下列变化中既有离子键断裂,又有共价键断裂的是( )| A. | NaOH溶于水 | B. | NH4HCO3受热分解 | C. | HCl溶于水 | D. | I2的升华 |
分析 活泼金属和活泼非金属之间易形成离子键,非金属元素之间易形成共价键,既有离子键断裂,又有共价键断裂,说明该物质中既含离子键又含共价键,以此解答该题.
解答 解:A.NaOH溶于水,只存在离子键的断裂,故A错误;
B.NH4HCO3受热分解生成氨气、二氧化碳和水,所以离子键和共价键都发生断裂,故B正确;
C.HCl中只含共价键,在水分子的作用下发生共价键电离,故C错误;
D.碘升华克服分子间作用力,故D错误.
故选B.
点评 本题考查化学键的变化,侧重考查分析判断能力,明确物质中存在的化学键及发生的变化是解本题关键,注意有化学键断裂不一定有化学键生成,如电解质溶于水,注意铵盐中都含有离子键,为易错点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.将106g Na2 CO3溶于1L水所得溶液与1mol Na2CO3溶于水稀释成1L的溶液相比,下列各量一定相等的是( )
| A. | 物质的量浓度 | B. | 溶液的密度 | C. | 溶质的质量 | D. | 溶质的质量分数 |
3.化学在生产生活中有广泛的应用,下列说法正确的是( )
| A. | 煤的气化和液化过程,都是物理变化 | |
| B. | 通过石油的裂解可得到汽油等多种产品 | |
| C. | 可用焦炭还原氧化铝的方法来冶炼铝 | |
| D. | 从海水中可以提取铀和重水等核原料 |
20.化学与生产、生活、社会密切相关,下列有关说法中正确的是( )
| A. | 海水中含有丰富的碘元素,因此碘被称为“海洋元素” | |
| B. | 地沟油经过加工处理后可用来制生物柴油和肥皂 | |
| C. | 可以利用氯化铁溶液的酸性清除铜镜表面的铜锈 | |
| D. | 大量使用薪柴为燃料,践行低碳生活 |
7.一定温度下,下列溶液的离子浓度关系式正确的是( )
| A. | pH相同的①CH3COONa②NaHCO3③NaClO三种溶液的c(Na+):①>②>③ | |
| B. | pH=a的氨水溶液,稀释10倍后,其pH=b,则a=b+1 | |
| C. | pH=2的H2C2O4溶液与pH=12的NaOH溶液任意比例混合:C(Na+)+c(H+)=c(OH-)+c(HC2O4-) | |
| D. | pH=5的H2S溶液中,c(H+)=c(HS-)=1×10-5mol•L-1 |
17.在下列反应中属于氧化还原反应且水做还原剂的是( )
| A. | Cl2+H2O=HCl+HClO | B. | 2H2O+2F2=4HF+O2 | ||
| C. | ICl+H2O=HCl+HIO | D. | 2Na+2H2O=2NaOH+H2↑ |
4.一种将燃料电池与电解池组合制备KMnO4的装置如图所示(电极甲、乙、丙、丁均为惰性电极).该装置工作时,下列说法不正确的是( )


| A. | 乙电极附近溶液的pH减小 | |
| B. | 电极丁的反应式为:MnO42--e-═MnO4- | |
| C. | KOH溶液的质量分数:c%>a%>b% | |
| D. | 导线中有2 mol电子通过时,理论上有2 mol K+移入阴极区 |
9.下列表示物质结构的化学用语或模型正确的是( )
| A. | 氟化氢的电子式: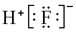 | B. | 白磷分子的球棍模型: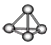 | ||
| C. | CO2分子的球棍模型: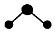 | D. | K+离子的结构示意图: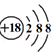 |
10.下列哪一种微粒的中心原子属于sp3杂化( )
| A. | BCl3 | B. | CO2 | C. | PCl3 | D. | HCHO |