题目内容
下列有关的离子方程式书写正确的是( )
A、向铜片中滴加浓硫酸并加热,有刺激性气体产生:Cu+4H++SO42-
| ||||
| B、向Ca(HCO3)2溶液中加入过量NaOH溶液,有白色沉淀生成:Ca2++2HCO3-+2OH-═CaCO3↓+2H2O+CO32- | ||||
| C、20mL 1.0mol/L的明矾溶液与10mL 3.5mol/L Ba(OH)2溶液混合充分反应有白色沉淀生成:3Ba2++6OH-+2Al3++3SO42-═3BaSO4↓+2Al(OH)3↓ | ||||
D、服用阿司匹林过量出现水杨酸( )中毒反应,可静脉注射NaHCO3溶液: )中毒反应,可静脉注射NaHCO3溶液: +2HCO3-→ +2HCO3-→ +2CO2↑+2H2O +2CO2↑+2H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A、浓硫酸不拆,应写成化学式;
B、过量NaOH溶液,Ca(HCO3)2溶液少量少的要符合组成之比;
C、20mL 1.0mol/L的明矾溶液与10mL 3.5mol/L Ba(OH)2溶液两的物质的量之比为4:7,设明矾为4mol,氢氧化钡为7mol,两者相比较硫酸根离子过量,铝离子和氢氧根离子完全反应生成等物质量的氢氧化铝,和偏铝酸根离子;
D、水杨酸中的羧基可以和碳酸氢钠发生反应,生成二氧化碳.
B、过量NaOH溶液,Ca(HCO3)2溶液少量少的要符合组成之比;
C、20mL 1.0mol/L的明矾溶液与10mL 3.5mol/L Ba(OH)2溶液两的物质的量之比为4:7,设明矾为4mol,氢氧化钡为7mol,两者相比较硫酸根离子过量,铝离子和氢氧根离子完全反应生成等物质量的氢氧化铝,和偏铝酸根离子;
D、水杨酸中的羧基可以和碳酸氢钠发生反应,生成二氧化碳.
解答:
解:A、浓硫酸不拆,应写成化学式,正确的离子方程式为Cu+2H2SO4
Cu2++SO2↑+2H2O+SO42-,故A错误;
B、过量NaOH溶液,Ca(HCO3)2溶液少量少的要符合组成之比,正确的离子方程式为Ca2++2HCO3-+2OH-═CaCO3↓+2H2O+CO32-,故B正确;
C、20mL 1.0mol/L的明矾溶液与10mL 3.5mol/L Ba(OH)2溶液两的物质的量之比为4:7,设明矾为4mol,氢氧化钡为7mol,两者相比较硫酸根离子过量,铝离子和氢氧根离子完全反应生成等物质量的氢氧化铝,和偏铝酸根离子,离子方程式为7Ba2++14OH-+4Al3++7SO42-═7BaSO4↓+2Al(OH)3↓+4H2O+2AlO2-,故C错误;
D、水杨酸中的羧基可以和碳酸氢钠发生反应,生成二氧化碳,正确的离子方程式为: +HCO3-→
+HCO3-→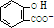 +CO2↑+H2O,故D错误;
+CO2↑+H2O,故D错误;
故选B.
| ||
B、过量NaOH溶液,Ca(HCO3)2溶液少量少的要符合组成之比,正确的离子方程式为Ca2++2HCO3-+2OH-═CaCO3↓+2H2O+CO32-,故B正确;
C、20mL 1.0mol/L的明矾溶液与10mL 3.5mol/L Ba(OH)2溶液两的物质的量之比为4:7,设明矾为4mol,氢氧化钡为7mol,两者相比较硫酸根离子过量,铝离子和氢氧根离子完全反应生成等物质量的氢氧化铝,和偏铝酸根离子,离子方程式为7Ba2++14OH-+4Al3++7SO42-═7BaSO4↓+2Al(OH)3↓+4H2O+2AlO2-,故C错误;
D、水杨酸中的羧基可以和碳酸氢钠发生反应,生成二氧化碳,正确的离子方程式为:
 +HCO3-→
+HCO3-→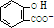 +CO2↑+H2O,故D错误;
+CO2↑+H2O,故D错误;故选B.
点评:本题考查离子方程式的书写,题目难度不大,注意从化学式、离子符号、电荷守恒以及是否符合反应实际的角度分析.

练习册系列答案
 天天练口算系列答案
天天练口算系列答案
相关题目
 一定温度下在2L容器内进行某一反应,气体X、气体Y的物质的量随反应时间变化的曲线如图.下列叙述中正确的是( )
一定温度下在2L容器内进行某一反应,气体X、气体Y的物质的量随反应时间变化的曲线如图.下列叙述中正确的是( )| A、反应的化学方程式为4X?Y |
| B、当t1=2时,用X表示该反应在2min内的平均反应速率为0.25mol/(L?min) |
| C、t2时,正反应速率等于逆反应速率 |
| D、t3时,Y浓度不再变化,反应达到平衡 |
丙烯酸的结构简式为CH2=CH-COOH,对其性质的描述不正确的是( )
| A、能与金属钠反应放出氢气 |
| B、能与溴水发生取代反应而使溴水褪色 |
| C、能使酸性高锰酸钾溶液褪色 |
| D、不能与新制氢氧化铜反应 |
能大量共存于同一溶液中,且当改变条件使水电离的c(H+)=10-13mol/L时,一定能发生反应的离子组是( )
| A、S2-、Na+、SO32-、Cl- |
| B、Ca2+、NH4+、SO42-、SiO32- |
| C、Na+、Ba2+、Cl-、HSO3- |
| D、Al3+、Na+、SO42-、NO3- |
某强碱性溶液中一定能大量共存的离子组是( )
| A、Na+、Ba2+、Cl-、NO3- |
| B、K+、Na+、NO3-、HCO3- |
| C、Na+、Fe2+、NO3-、SCN- |
| D、Na+、Ca2+、SiO32-、Cl- |
下列分子中,既含有σ键又含有π键的是( )
| A、CH4 |
| B、HCl |
| C、CH2═CH2 |
| D、F2 |
 有机物M的结构简式如图所示.
有机物M的结构简式如图所示. P4具有正四面体结构,它在Cl2中燃烧可生成PCl5和PCl3两种产物,经测定在PCl5中P-Cl与PCl3中的P-Cl键能是不同的.若PCl5中P-Cl键的键能为akJ?mol-1,而PCl3中P-Cl键的键能为1.2akJ?mol-1.
P4具有正四面体结构,它在Cl2中燃烧可生成PCl5和PCl3两种产物,经测定在PCl5中P-Cl与PCl3中的P-Cl键能是不同的.若PCl5中P-Cl键的键能为akJ?mol-1,而PCl3中P-Cl键的键能为1.2akJ?mol-1.