题目内容
6.下列说法不正确的是( )| A. | 下列转化均能一步实现:粗硅$→_{高温}^{Cl_{2}}$SiCl4$→_{高温}^{H_{2}}$Si | |
| B. | 元素C的单质只存在金刚石和石墨两种同素异形体 | |
| C. | 硬度:晶体硅<金刚石 | |
| D. | 高温下用焦炭还原SiO2制取粗硅 |
分析 A.粗硅和氯气反应生成四氯化硅,四氯化硅和氢气反应生成硅和水;
B.C元素的单质存在多种同素异形体;
C.原子晶体中,键长越短,键能越大,则硬度越大;
D.碳还原二氧化硅生成硅和一氧化碳;
解答 解:A.粗硅和氯气反应生成四氯化硅,四氯化硅和氢气反应生成硅和水,转化均能一步实现,故A正确;
B.元素C除存在金刚石和石墨外,还存在足球烯(C60)等同素异形体,故B错误;
C.晶体硅与金刚石都为原子晶体,其中化学键的键长为:C-C<Si-Si,原子晶体中,键长越短,键能越大,则硬度越大,故C正确;
D工业上在.高温下用焦炭还原SiO2制取粗硅,碳和二氧化硅反应生成硅和一氧化碳,故D正确;
故选B.
点评 本题考查了硅、二氧化硅等物质性质和结构的分析判断,掌握基础是解题关键,题目难度不大.

练习册系列答案
相关题目
16.下列物质中,不能用作漂白剂的是( )
| A. | H2SO4(浓) | B. | O3 | C. | Ca(ClO)2 | D. | SO2 |
17.某化学探究小组拟用废铜屑制取Cu(NO3)2,并探究其化学性质.
I.如图1,用浓HNO3,和过量的废铜屑充分反应制硝酸铜溶液.
(1)写出铜与浓硝酸反应的离子方程式Cu+4H++2NO3-=Cu2++2NO2↑+2H2O.
(2)①装置中NaOH溶液的作用是吸收氮氧化物,防止污染空气.
②欲从反应后的溶液中得到硝酸铜晶体,实验操作步骤是蒸发浓缩、冷却结晶、过滤.
③你认为此装置是否合理,并说明原因不合理,密闭体系中立即产生大量气体,会有安全隐患;或者合理,慢慢挤压,胶头滴管控制反应速率,使NaOH溶液及时吸收NO2.
如果不合理,同时在原装置上改进;如果合理,只需说明原因.
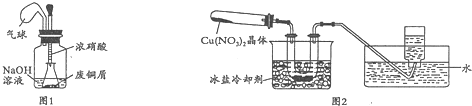
Ⅱ.为了探究Cu(NO3)2的热稳定性,探究小组按图2装置进行实验.(图中铁架台、铁夹和加热仪器均略去)
【实验装置】
【实验操作及现象】往试管中放入研细的无水Cu(NO3)2晶体并加热,观察到试管中有红棕色气体生成,最终残留黑色粉末;用U型管除去红棕色气体,在集气瓶中收集到无色气体.
【解释与结论】
(3)①红棕色气体是NO2.
②根据现象判断Cu(NO3)2在加热条件下可以分解,其化学反应方程式为2Cu(NO3)2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+4NO2↑+O2↑.
Ⅲ.利用Cu(NO3)2制备浅绿色的碱式碳酸铜[CuCO3•Cu(OH)2].
向大试管中加入一定量的碳酸钠溶液和硝酸铜溶液,水浴加热,用0.4mol•L-1的NaOH溶液调节pH至8.5,振荡、静置、过滤、洗涤、干燥,得到样品.
【实验数据】反应温度对样品的影响
(4)滤液中可能含有CO32-,写出检验CO32-的方法取少量滤液置于试管中,加入足量稀盐酸,将产生的气体通入澄清石灰水,溶液变浑浊,说明含碳酸根离子.
(5)95℃时,样品颜色发暗的原因:含有黑色的氧化铜.
(6)70℃时,实验得到2.38g样品,取此样品加热至分解完全(杂质不分解),得到1.76g固体,此样品中碱式碳酸铜的质量分数是93.3%.
I.如图1,用浓HNO3,和过量的废铜屑充分反应制硝酸铜溶液.
(1)写出铜与浓硝酸反应的离子方程式Cu+4H++2NO3-=Cu2++2NO2↑+2H2O.
(2)①装置中NaOH溶液的作用是吸收氮氧化物,防止污染空气.
②欲从反应后的溶液中得到硝酸铜晶体,实验操作步骤是蒸发浓缩、冷却结晶、过滤.
③你认为此装置是否合理,并说明原因不合理,密闭体系中立即产生大量气体,会有安全隐患;或者合理,慢慢挤压,胶头滴管控制反应速率,使NaOH溶液及时吸收NO2.
如果不合理,同时在原装置上改进;如果合理,只需说明原因.

Ⅱ.为了探究Cu(NO3)2的热稳定性,探究小组按图2装置进行实验.(图中铁架台、铁夹和加热仪器均略去)
【实验装置】
【实验操作及现象】往试管中放入研细的无水Cu(NO3)2晶体并加热,观察到试管中有红棕色气体生成,最终残留黑色粉末;用U型管除去红棕色气体,在集气瓶中收集到无色气体.
【解释与结论】
(3)①红棕色气体是NO2.
②根据现象判断Cu(NO3)2在加热条件下可以分解,其化学反应方程式为2Cu(NO3)2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+4NO2↑+O2↑.
Ⅲ.利用Cu(NO3)2制备浅绿色的碱式碳酸铜[CuCO3•Cu(OH)2].
向大试管中加入一定量的碳酸钠溶液和硝酸铜溶液,水浴加热,用0.4mol•L-1的NaOH溶液调节pH至8.5,振荡、静置、过滤、洗涤、干燥,得到样品.
【实验数据】反应温度对样品的影响
| 实验序号 | 1 | 2 | 3 | 4 |
| 温度/℃ | 35 | 50 | 70 | 95 |
| 样品颜色 | 深蓝色 | 深蓝色 | 浅绿色 | 暗蓝色 |
| 样品中碱式碳酸铜的质量分数/% | 90.9 | 92.7 | x | 92.0 |
(5)95℃时,样品颜色发暗的原因:含有黑色的氧化铜.
(6)70℃时,实验得到2.38g样品,取此样品加热至分解完全(杂质不分解),得到1.76g固体,此样品中碱式碳酸铜的质量分数是93.3%.
14.下列说法不正确的是( )
| A. | 医疗上常用75%的酒精杀菌消毒 | |
| B. | 由于分子间氢键的存在,NH3易液化,H2O常温下呈液态 | |
| C. | 雾霾公益调查纪录片《穹顶之下》的发布引起了人们的关注,雾霾属于胶体 | |
| D. | 氢气是理想的绿色能源,贮氢合金的发现和应用解决了氢气贮存运输的难题,贮氢金属与氢气发生化学反应,形成氢化物,达到贮存氢气的目的 |
1.下列过程与蛋白质变性无关的是( )
| A. | 用煮沸的方法可使医疗器械消毒 | |
| B. | 用福尔马林保存生物标本 | |
| C. | 鸡蛋白溶液里加入饱和硫酸铵溶液,可以观察到有沉淀析出 | |
| D. | 鸡蛋白溶液里加入少量乙酸铅溶液,可以观察到有沉淀生成 |
8.下列关于胶体的认识,错误的是( )
| A. | 是否能形成丁达尔效应是胶体和溶液最本质的区别 | |
| B. | 胶体微粒具有较大的表面积,能吸附阳离子或阴离子,故在电场作用下会产生电泳现象 | |
| C. | “雨后彩虹”“海市蜃楼”既是一种自然现象又是光学现象,也与胶体的知识有关 | |
| D. | 除去Fe(OH)3胶体中的FeCl3,可将混合物装入半透膜中,放入蒸馏水里 |
6.下列有关试剂的保存方法,错误的是( )
| A. | 浓硝酸保存在无色玻璃试剂瓶中 | |
| B. | 少量的钠保存在煤油中 | |
| C. | NaOH溶液保存在具有玻璃塞的玻璃试剂瓶中 | |
| D. | 新制氯水保存在棕色玻璃试剂瓶中 |
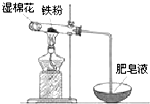 铁是日常生活中用途最广、用量最大的金属材料.
铁是日常生活中用途最广、用量最大的金属材料.