题目内容
13.下列条件下,两瓶气体所含的原子数一定相等的是( )| A. | 同质量、不同密度的O2和O3 | B. | 同温度、同体积的CO和N2 | ||
| C. | 同体积、同密度的N2O和CO2 | D. | 同压强、同体积的SO2和NO2 |
分析 两瓶气体所含的原子数一定相等,则原子的物质的量相同,结合n=$\frac{m}{M}$及物质的构成解答.
解答 解:A.同质量的O2和O3,O原子的物质的量相同,则数目相同,故A正确;
B.同温度、同体积的CO和N2,压强未知,则物质的量的关系不确定,原子数不一定相等,故B错误;
C.同体积、同密度的N2O和CO2,质量相同、二者的摩尔质量相同,均由2个原子构成分子,则原子的物质的量相同,则含有的原子数目相同,故C正确;
D.同压强、同体积的SO2和NO2,温度未知,则物质的量的关系不确定,原子数不一定相等,故D错误;
故选AC.
点评 本题考查物质的量的有关计算及阿伏伽德罗定律,注意阿伏伽德罗定律中pV=nRT中各量的关系,熟悉n=$\frac{m}{M}$即可解答,题目难度不大.

练习册系列答案
相关题目
5.下列说法正确的是( )
| A. | 催化剂对反应热和反应的活化能均无影响 | |
| B. | 中和热△H=-57.3kJ/mol,则0.1mol稀硫酸与足量的氢氧化钡溶液反应放热11.46kJ | |
| C. | 焓变是指1mol物质参加反应时的能量变化,在等压时,反应热等于焓变 | |
| D. | 破坏生成物化学键所需总能量小于破坏反应物化学键所需总能量的反应是吸热反应 |
4.下列关于资源开发利用的说法,不正确的是( )
| A. | 石油经分馏后得到的汽油是纯净物 | |
| B. | 煤的干馏是复杂的物理化学变化,石油分馏是物理变化 | |
| C. | 从海水中得到无水MgCl2,电解熔融MgCl2制取金属镁 | |
| D. | 天然油脂是混合物,所以天然油脂没有固定的熔点和沸点 |
18.x、y为两种短周期元素的原子,x的阴离子与y的阳离子具有相同的电子层结构,由此可知( )
| A. | x的原子半径大于y的原子半径 | |
| B. | x的电负性大于y的电负性 | |
| C. | x阴离子的半径小于y阳离子的半径 | |
| D. | x的第一电离能大于y 的第一电离能 |
5.钾和另一种碱金属组成的合金18.0g与足量的水完全反应,产生氢气1g,则合金中的另一种金属是( )
| A. | Cs | B. | Rb | C. | Na | D. | Li |
2.对于Fe-Cu-稀H2SO4组成的原电池中当有4mol电子通过导线时,则下列说法正确的是( )
| A. | 铁片溶解了56g | B. | 铜片上析出标准状况下22.4L气体 | ||
| C. | 电解质溶液的pH逐渐减小 | D. | SO42-移向Fe电极 |
3.蘸有浓硫酸的纸片会发黑,主要是浓硫酸具有( )
| A. | 吸水性 | B. | 氧化性 | C. | 脱水性 | D. | 酸性 |
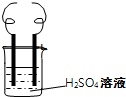 用电极a(铁丝)、电极b(铜丝)和H2SO4溶液可以构成原电池或电解池,如图所示.
用电极a(铁丝)、电极b(铜丝)和H2SO4溶液可以构成原电池或电解池,如图所示.