题目内容
2. 金属是日常生活和工农业生产中广泛使用的材料.恰当的金属防腐方法是延长金属材料使用寿命的前提.
金属是日常生活和工农业生产中广泛使用的材料.恰当的金属防腐方法是延长金属材料使用寿命的前提.(1)烤蓝是钢铁零件表面处理的防腐蚀的工艺,其原理就是在钢铁表面生成一定厚度和强度的致密的氧化物薄膜(Fe3O4),方法之一是在碱性条件下用NaNO2、NaNO3分别将Fe氧化为亚铁酸钠(Na2FeO2)、铁酸钠(Na2Fe2O4),这两个反应要发生除分别需要NaNO2、NaNO3试剂外,还需要的试剂为NaOH(填化学式);上述两个反应的生成物亚铁酸钠与铁酸钠反应生成Fe3O4氧化膜,反应的化学方程式为2H2O+Na2FeO2+Na2Fe2O4=4NaOH+Fe3O4.
(2)锌酸钾(K2ZnO2)的碱性溶液作为电解质溶液可以镀锌,该工艺中镀件为阴极(选填“阳极”或“阴极”),阳极电极反应式为Zn+4OH--2e-═ZnO22-+2H2O,阴极电极反应式为ZnO22-+2H2O+2e-=Zn+4OH-.
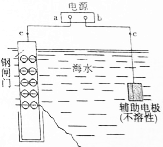
(3)外加电流保护法是金属防腐的重要方法,其原理如图所示.a为电源负(选填“正”或“负”)极,写出一种符合“辅助电极”的物质名称石墨.
分析 (1)这两个反应必须在碱性条件下反应,结合元素守恒确定还需要试剂;根据反应物、生成物书写方程式;
(2)镀层为阳极、镀件为阴极,阳极上Zn失电子和氢氧根离子反应生成锌酸根离子和水,阴极上锌酸根离子失电子生成Zn;
(3)外加电流保护法是金属防腐的重要方法,钢闸门作阴极被保护,则钢闸门应该连接原电池负极;辅助电极应该具有导电性且不易被氧化.
解答 解:(1)这两个反应必须在碱性条件下反应,结合元素守恒确定还需要试剂为NaOH;根据反应物、生成物书写方程式为2H2O+Na2FeO2+Na2Fe2O4=4NaOH+Fe3O4,故答案为:NaOH;2H2O+Na2FeO2+Na2Fe2O4=4NaOH+Fe3O4;
(2)镀层为阳极、镀件为阴极,阳极上Zn失电子和氢氧根离子反应生成锌酸根离子和水,阴极上锌酸根离子失电子生成Zn,电极反应式为ZnO22-+2H2O+2e-=Zn+4OH-,故答案为:阴极;ZnO22-+2H2O+2e-=Zn+4OH-;
(3)外加电流保护法是金属防腐的重要方法,钢闸门作阴极被保护,则钢闸门应该连接原电池负极,则a为负极;辅助电极应该具有导电性且不易被氧化,可以用石墨,故答案为:负极;石墨.
点评 本题考查电解原理,为高频考点,侧重考查学生分析判断能力,涉及电解原理、金属腐蚀与防护、电镀等知识点,难点是反应方程式的书写,要结合电解质溶液酸碱性书写,题目难度不大.

练习册系列答案
相关题目
13.下列叙述I和II均正确并有因果关系的是( )
| 选项 | 叙述I | 叙述II |
| A | 实验室常用Al2(SO4)3溶液与氨水溶液制备Al(OH)3沉淀 | Al(OH)3不溶于碱 |
| B | NaHCO3为强碱弱酸盐 | NaHCO3溶液显碱性 |
| C | SO2具有氧化性 | SO2可用品红溶液检验 |
| D | 明矾水解产生具有吸附性的胶体 | 明矾可作自来水消毒 |
| A. | A | B. | B | C. | C | D. | D |
10.钢铁腐蚀在生活和生产中相当普遍.下列措施能防止钢铁腐蚀的是( )
| A. | 将输油铁管埋在潮湿.疏松的土壤中 | |
| B. | 经常用自来水冲洗钢铁制品 | |
| C. | 将输送自来水的铁管表面镀锌 | |
| D. | 把钢铁雕塑焊接在铜质基座上 |
14.将下列铁的化合物溶于盐酸,滴加KSCN溶液后颜色变化最不明显的是( )
| A. | FeO | B. | Fe3O4 | C. | Fe2O3 | D. | Fe(OH)3 |
1.某化学课外小组的同学通过实验探究认识化学反应速率和化学反应限度.
(1)实验一:探究温度和浓度对反应速率的影响
实验原理及方案:在酸性溶液中,碘酸钾( KIO3)和亚硫酸钠可发生反应生成碘,反应原理是2IO3-+5SO32-+2H+═I2+5SO42-+H2O,生成的碘可用淀粉溶液检验,根据出现蓝色所需的时间来衡量该反应的速率.
则V1=40mL,V2=10mL.
(2)实验二:探究KI和FeCl3混合时生成KCl、I2和FeCl2的反应存在一定的限度.
实验步骤:
i.向5mL0.1mol/L KI溶液中滴加5~6滴0.1mol/L FeCI3溶液,充分反应后,将所得溶液分成甲、乙、丙三等份;
ii.向甲中滴加CCl4,充分振荡;
iii.向乙中滴加试剂X.
①将KI和FeCl3反应的离子方程式补充完整.
2I-+2Fe3+?1I2+2Fe2+
②步骤iii中,试剂X是KSCN溶液.
③步骤ii和iii中的实验现象说明KI和FeCl3混合时生成KCI、I2和FeCl2的反应存在一定的限度,该实验现象是ii中可观察到溶液分层,下层呈现紫红色,iii中可观察到溶液变红.
(1)实验一:探究温度和浓度对反应速率的影响
实验原理及方案:在酸性溶液中,碘酸钾( KIO3)和亚硫酸钠可发生反应生成碘,反应原理是2IO3-+5SO32-+2H+═I2+5SO42-+H2O,生成的碘可用淀粉溶液检验,根据出现蓝色所需的时间来衡量该反应的速率.
| 实验 序号 | 0.01mol/L KIO3酸性溶液 (含淀粉)的体积/mL | 0.01mol/L Na2SO3溶 液的体积/mL | 水的体 积/mL | 实验温 度/℃ | 出现蓝色 的时间/s |
| ① | 5 | 5 | V1 | 0 | |
| ② | 5 | 5 | 40 | 25 | |
| ③ | 5 | V2 | 35 | 25 |
(2)实验二:探究KI和FeCl3混合时生成KCl、I2和FeCl2的反应存在一定的限度.
实验步骤:
i.向5mL0.1mol/L KI溶液中滴加5~6滴0.1mol/L FeCI3溶液,充分反应后,将所得溶液分成甲、乙、丙三等份;
ii.向甲中滴加CCl4,充分振荡;
iii.向乙中滴加试剂X.
①将KI和FeCl3反应的离子方程式补充完整.
2I-+2Fe3+?1I2+2Fe2+
②步骤iii中,试剂X是KSCN溶液.
③步骤ii和iii中的实验现象说明KI和FeCl3混合时生成KCI、I2和FeCl2的反应存在一定的限度,该实验现象是ii中可观察到溶液分层,下层呈现紫红色,iii中可观察到溶液变红.
2.已知FeSO4在不同条件下分解得到的产物不同,可能是FeO和SO3,也可能是Fe2O3、SO3和SO2.某研究小组探究在酒精喷灯加热条件下FeSO4分解的气体产物.已知SO3的熔点是16.8℃,沸点是44.8℃.
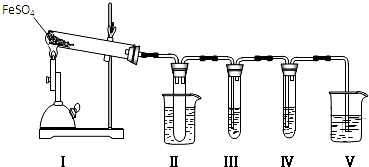
(1)装置Ⅱ的试管中不装任何试剂,其作用是防止溶液倒吸入装置Ⅰ中(或安全瓶),试管浸泡在50℃的水浴中,目的是防止SO3液化或凝固;
(2)装置Ⅲ和装置Ⅳ的作用是探究本实验气体产物成分.请完成实验设计,填写检验试剂、预期现象与结论.限选试剂:3mol•L-1 H2SO4、6mol•L-1 NaOH、0.5mol•L-1 BaCl2、0.5mol•L-1 Ba(NO3)2、0.01mol•L-1酸性KMnO4溶液、0.01mol•L-1溴水.
(3)也有同学认为可以通过检验试管中残留固体证明分解产物.方案如下:
取适量残留固体于试管中,加入足量稀硫酸,将所得溶液分为两份.向第一份溶液中滴加硫氰化钾溶液,若变红,证明分解产物中有氧化铁;向第二份溶液滴加酸性高锰钾溶液,若褪色证明分解产物中有氧化亚铁.
①写出第一份溶液中反应的离子方程式Fe3++3SCN-?Fe(SCN)3;
②有同学认为高锰酸钾溶液褪色不能说明分解产物有氧化亚铁,理由是如果FeSO4未完全分解,溶液里也存在Fe2+.

(1)装置Ⅱ的试管中不装任何试剂,其作用是防止溶液倒吸入装置Ⅰ中(或安全瓶),试管浸泡在50℃的水浴中,目的是防止SO3液化或凝固;
(2)装置Ⅲ和装置Ⅳ的作用是探究本实验气体产物成分.请完成实验设计,填写检验试剂、预期现象与结论.限选试剂:3mol•L-1 H2SO4、6mol•L-1 NaOH、0.5mol•L-1 BaCl2、0.5mol•L-1 Ba(NO3)2、0.01mol•L-1酸性KMnO4溶液、0.01mol•L-1溴水.
| 检验试剂 | 预期现象和结论 |
| 装置Ⅲ的试管中加入0.5mol.L-1BaCl2. | 产生大量白色沉淀,证明气体产物中含有SO3. |
| 装置Ⅳ的试管中加入0.01mol.L-1酸性KMnO4溶液(或0.0lmol.L-1溴水). |
取适量残留固体于试管中,加入足量稀硫酸,将所得溶液分为两份.向第一份溶液中滴加硫氰化钾溶液,若变红,证明分解产物中有氧化铁;向第二份溶液滴加酸性高锰钾溶液,若褪色证明分解产物中有氧化亚铁.
①写出第一份溶液中反应的离子方程式Fe3++3SCN-?Fe(SCN)3;
②有同学认为高锰酸钾溶液褪色不能说明分解产物有氧化亚铁,理由是如果FeSO4未完全分解,溶液里也存在Fe2+.
