题目内容
下列说法正确的是( )
| A、胶体与其它分散系的本质区别是有丁达尔效应,而其它分散系没有 |
| B、胶体粒子的直径小于1nm |
| C、丁达尔效应可用于鉴别胶体和溶液 |
| D、胶粒能通过滤纸,也能通过半透膜 |
考点:胶体的重要性质
专题:溶液和胶体专题
分析:A、胶体的分散质微粒直径大小是胶体区别于其它分散系的本质特征所在;
B、粒子的直径在1-100nm的为胶体;
C、胶体具有丁达尔效应;
D、胶粒不能通过半透膜.
B、粒子的直径在1-100nm的为胶体;
C、胶体具有丁达尔效应;
D、胶粒不能通过半透膜.
解答:
解:A、胶体区别于其它分散系的本质是胶体分散质微粒直径的大小,分散质粒子直径在1nm~100nm之间的分散系属于胶体,故A错误;
B、粒子的直径在1-100nm的为胶体,小于1nm的为溶液,故B错误;
C、胶体具有丁达尔效应,溶液没有丁达尔效应,所以丁达尔效应可用于鉴别胶体和溶液,故C正确;
D、胶粒较小能通过滤纸,但是胶粒不能通过半透膜,故D错误;
故选C.
B、粒子的直径在1-100nm的为胶体,小于1nm的为溶液,故B错误;
C、胶体具有丁达尔效应,溶液没有丁达尔效应,所以丁达尔效应可用于鉴别胶体和溶液,故C正确;
D、胶粒较小能通过滤纸,但是胶粒不能通过半透膜,故D错误;
故选C.
点评:本题考查了分散系的分类依据、胶体的鉴别等,侧重于基础知识的考查,题目难度不大.

练习册系列答案
 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案
相关题目
下列说法正确的是( )
| A、氧化还原反应的本质是元素化合价发生变化 |
| B、还原剂是一种能够得到电子的物质 |
| C、物质所含元素化合价降低的反应是氧化反应 |
| D、氧化反应和还原反应是同时发生的 |
在密闭容器中充入4molSO2和3molO2,一定条件下平衡:2SO2(g)+O2(g)?2SO3(g)△H=-a kJ/mol,反应中测得SO2的转化率为90%,则在此条件下反应放出的热量( )
| A、1.8a kJ |
| B、a kJ |
| C、2a kJ |
| D、0.9a kJ |
用NA表示阿伏加德罗常数的数值,下列叙述正确的是( )
| A、标准状况下,22.4L H2含有的原子数为NA |
| B、等质量的O2和O3中所含分子数相等 |
| C、常温常压下,14g N2含有电子数为7NA |
| D、等质量的CO与CO2中所含碳原子数之比为7:11 |
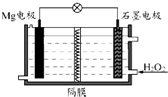 Mg-H2O2电池可用于驱动无人驾驶的潜航器.该电池以海水为电解质溶液,示意图如图所示.该电池工作时,下列说法错误的是( )
Mg-H2O2电池可用于驱动无人驾驶的潜航器.该电池以海水为电解质溶液,示意图如图所示.该电池工作时,下列说法错误的是( )| A、Mg电极是该电池的负极 |
| B、溶液中Cl-向石墨电极移动 |
| C、该装置中电子从Mg电极流向石墨电极 |
| D、H2O2在石墨电极上发生还原反应 |
将标况下的NH3溶于水中,得到密度为b g?cm-3的氨水a g,物质的量浓度为c mol?L-1,则溶于水中的NH3的体积是( )
A、
| ||
B、
| ||
C、
| ||
D、
|
在体积一定的密闭容器中加入一定量的物质A、B、C,在一定条件下发生反应建立的化学平衡:aA(g)+bB(g)?xC(g),符合如图所示的关系(c%表示平衡混合气中产物C的百分含量,T表示温度,p表示压强).在图中,Y轴是指( )
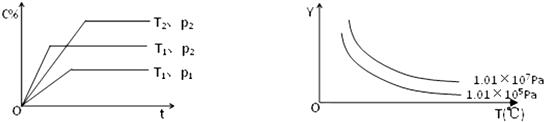

| A、反应物A的百分含量 |
| B、反应体系内分子的总数目 |
| C、平衡混合气体的密度 |
| D、平衡混合气体的平均摩尔质量 |
在一定温度下,固定容积中发生可逆反应:N2(g)+3H2(g)?2NH3(g),下列情况一定能说明此反应达到平衡状态的是( )
| A、体系的压强或混合气体密度不再改变 |
| B、各物质的浓度保持不变 |
| C、反应速率υ(N2):υ(H2):υ(NH3)=1:3:2 |
| D、单位时间内消耗0.1molN2,同时消耗0.3mol H2 |
由下列反应:Cu+2FeCl3→2FeCl2+CuCl2,CuCl2+Fe→FeCl2+Cu,确定Fe2+、Fe3+、Cu2+的氧化性强弱顺序为( )
| A、Fe2+>Cu2+>Fe3+ |
| B、Fe3+>Cu2+>Fe2+ |
| C、Fe3+>Fe2+>Cu2+ |
| D、Fe2+>Fe3+>Cu2+ |