题目内容
根据元素周期表和元素周期律分析下面的推断,其中错误的是( )
| A、砹的氢化物不稳定 |
| B、硒化氢比硫化氢稳定 |
| C、氢氧化锶比氢氧化钙的碱性强 |
| D、铍的原子失电子能力比镁弱 |
考点:同一主族内元素性质递变规律与原子结构的关系
专题:元素周期律与元素周期表专题
分析:A、同主族元素的原子,从上到下氢化物的稳定性逐渐减弱;
B、同主族元素的原子,从上到下氢化物的稳定性逐渐减弱;
C、同主族元素的原子,从上到下其最高价氧化物对应水化物的碱性逐渐增强;
D、同主族元素的原子,从上到下失电子能力逐渐增强.
B、同主族元素的原子,从上到下氢化物的稳定性逐渐减弱;
C、同主族元素的原子,从上到下其最高价氧化物对应水化物的碱性逐渐增强;
D、同主族元素的原子,从上到下失电子能力逐渐增强.
解答:
解:A、同主族元素的原子,从上到下氢化物的稳定性逐渐减弱,碘的氢化物不稳定,所以砹(At)的氢化物不稳定,故A正确;
B、同主族元素的原子,从上到下氢化物的稳定性逐渐减弱,所以硒(Se)化氢不如硫化氢稳定,故B错误;
C、同主族元素的原子,从上到下其最高价氧化物对应水化物的碱性逐渐增强,所以氢氧化锶[(Sr(OH)2]比氢氧化钙的碱性强,故C正确;
D、同主族元素的原子,从上到下失电子能力逐渐增强,所以铍(Be)的原子失电子能力比镁弱,故D正确.
故选B.
B、同主族元素的原子,从上到下氢化物的稳定性逐渐减弱,所以硒(Se)化氢不如硫化氢稳定,故B错误;
C、同主族元素的原子,从上到下其最高价氧化物对应水化物的碱性逐渐增强,所以氢氧化锶[(Sr(OH)2]比氢氧化钙的碱性强,故C正确;
D、同主族元素的原子,从上到下失电子能力逐渐增强,所以铍(Be)的原子失电子能力比镁弱,故D正确.
故选B.
点评:本题考查学生元素周期律的应用知识,侧重于考查同主族元素性质的递变规律,难度不大.

练习册系列答案
 金博士一点全通系列答案
金博士一点全通系列答案
相关题目
下列反应中必须加入氧化剂才能进行的是( )
| A、Cl2→Cl- |
| B、Zn2+→Zn |
| C、H2→H2O |
| D、CuO→CuCl2 |
最近,科学家用巨型计算机进行模拟后确认,由60个N 原子可结合成N60分子,N60变成N2时放出巨大能量,下列说法中不正确的是( )
| A、N60与N2都是氮的同素异形体 |
| B、N60 转化为N2属化学变化 |
| C、N2的相对分子质量为840,属高分子化合物 |
| D、N60变为 N2的反应是放热反应,说明N2比N60更稳定 |
下列化合物中,在常温常压下以液态形式存在的是( )
| A、丙烯 | B、乙烯 | C、甲醇 | D、丁烷 |
下列表达方式错误的是( )
A、氟化钠的电子式 |
B、氯原子的结构示意图: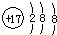 |
| C、CO2分子的结构式:O=C=O |
D、甲烷的电子式  |
下列各组离子,在溶液中能大量共存的是( )
| A、H+、Na+、NO3-、Fe2+ |
| B、Na+、K+、NH4+、H+ |
| C、K+、NH4+、NO3-、OH- |
| D、H+、K+、NO3-、CO32- |
关于元素周期表,下列叙述中不正确的是( )
| A、在金属与非金属的交界处可以找到良好的半导体材料 |
| B、在过渡元素中可以寻找催化剂及耐高温和耐腐蚀的合金材料 |
| C、在元素周期表的左下角可以寻找制备新型农药材料的元素 |
| D、目前使用的元素周期表中,最长的周期含有32种元素 |
