题目内容
18.现有带活塞的密闭容器A和B,一定温度时容器A装入碘化氢气体、容器B装入二氧化氮气体,使其体积相等.当温度不变时,缓缓压缩两容器,使两容器的压强均为原来的4倍,此时两容器内气体的体积关系正确的是(所有物质始终为气态)( )| A. | A=B | B. | A<B | C. | 无法判断 | D. | A>B |
分析 A中平衡为:2HI(g)?H2(g)+I2(g).B中平衡为:2NO2(g)?N2O4(g),加压后A中反应前后气体体积不变不发生平衡移动,B气体体积减小,向正反应方向移动导致B的体积再减小;
解答 解:带活塞的密闭容器A和B,A中化学平衡为:2HI(g)?H2(g)+I2(g),是气体体积不变的反应,
B中化学平衡为:2NO2(g)?N2O4(g),是气体体积减小的反应,
当温度不变时,缓缓压缩两容器,使两容器的压强均为原来的4倍,加压后A中反应前后气体体积不变不发生平衡移动,体积为原来的$\frac{1}{4}$,B中平衡向正反应方向移动导致B的体积再减小,体积小于原来的$\frac{1}{4}$,则最后气体容器体积A>B,
故选D.
点评 本题考查了化学平衡影响因素分析,主要是反应特征和平衡移动原理的理解应用,题目难度中等.

练习册系列答案
相关题目
8.化学与生产、生活、社会密切相关,下列说法中正确的是( )
| A. | 甲烷、乙烯和苯在工业上都可通过石油分馏得到 | |
| B. | 钢铁在潮湿的空气中放置,易发生化学腐蚀而生锈 | |
| C. | 绿色化学的核心是从源头上消除工业生产对环境的污染 | |
| D. | 汽油、柴油和植物油都是碳氢化合物 |
6.用下列实验装置进行相应实验,设计正确且能达到实验目的是( )
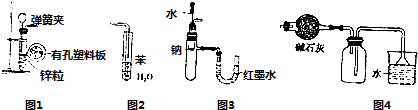

| A. | 用图1所示装置制取少量H2 | |
| B. | 用图2所示装置吸收氨气以防止倒吸 | |
| C. | 用图3所示装置验证Na和水反应的热效应 | |
| D. | 用图4所示装置可用于干燥、收集氯化氢气体 |
3.对于可逆反应mA+nB?pC正反应的反应热为△H.分别改变温度、压强、B的物质的量导致平衡常数(K)、A的转化率(a%)、A的物质的量浓度[c(A)]发生如图所示的变化.根据图中变化情况,以下结论正确的是( )
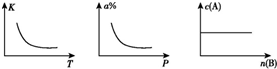

| A. | m+n<p,△H>0 A、B、C均为气体 | B. | m<p△H<0 A、C均为气体 | ||
| C. | n>p,△H>0 B、C均为气体 | D. | m>p,△H<0 A、C均为气体 |
1. Bodensteins研究了下列反应:2HI(g)?H2(g)+I2(g)△H═11kJ•mol-1.在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如表:
Bodensteins研究了下列反应:2HI(g)?H2(g)+I2(g)△H═11kJ•mol-1.在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如表:
由实验数据计算得到v正~x(HI)和v逆~x(H2)的关系可用如图表示.当改变条件,再次达到平衡时,下列有关叙述不正确的是( )
 Bodensteins研究了下列反应:2HI(g)?H2(g)+I2(g)△H═11kJ•mol-1.在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如表:
Bodensteins研究了下列反应:2HI(g)?H2(g)+I2(g)△H═11kJ•mol-1.在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如表:| t/min | 0 | 20 | 40 | 60 | 80 | 120 |
| x(HI) | 1 | 0.91 | 0.85 | 0.815 | 0.795 | 0.784 |
| x(HI) | 0 | 0.60 | 0.73 | 0.773 | 0.780 | 0.784 |
| A. | 若升高温度到某一温度,再次达到平衡时,相应点可能分别是A、E | |
| B. | 若再次充入a mol HI,则达到平衡时,相应点的横坐标值不变,纵坐标值增大 | |
| C. | 若改变的条件是增大压强,再次达到平衡时,相应点与改变条件前相同 | |
| D. | 若改变的条件是使用催化剂,再次达到平衡时,相应点与改变条件前不同 |
 (1)已知1molSO2(g)生成1molSO3(g)的能量变化如图所示,回答下列问题:
(1)已知1molSO2(g)生成1molSO3(g)的能量变化如图所示,回答下列问题: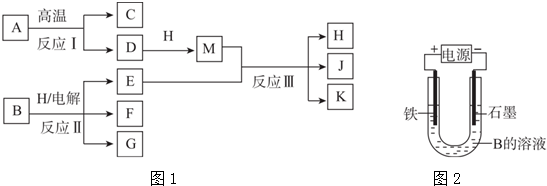
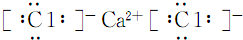 .
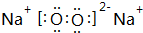
.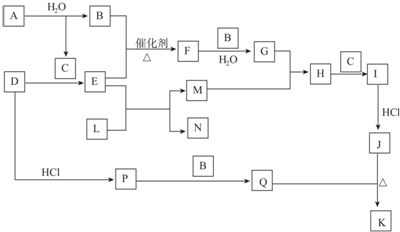
 ,D的化学式(NH4)2S.
,D的化学式(NH4)2S.