题目内容
在花瓶中加入“鲜花保鲜剂”,能延长鲜花的寿命.
(1)现有一种无色的鲜花营养液,可能由硝酸钙、碳酸钾、硝酸钾、氯化钾中的一种或几种物质组成,为探究其成分,某同学设计并完成了如图所示的实验.

根据以上实验,请你填空.
①由实验1可确定原营养液中一定没有的物质是 (填化学式),写出生成白色沉淀的离子方程式是 .
②若测得原营养液中K+、Cl-的数目之比为2:1,则原营养液是由 种溶质配制成的.
③某同学用氯化钙、硝酸钾、氯化钾配成的营养液中K+、Cl-、NO3-的数目之比为2:5:1,则所用硝酸钾和氯化钙的物质的量之比是 .
(2)下表是500mL某“鲜花保鲜剂”中含有的成分,阅读后回答下列问题.
①“鲜花保鲜剂”中蔗糖的物质的量浓度为 .
②配制该500mL“鲜花保鲜剂”所需的玻璃仪器除了烧杯、玻璃棒、量筒外还有 .
③在溶液配制过程中,下列操作能使配制结果偏小的是 .
A.定容时仰视容量瓶刻度线
B.容量瓶在使用前未干燥,里面有少量蒸馏水
C.移液时,液体不小心从外壁流出
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理.
(1)现有一种无色的鲜花营养液,可能由硝酸钙、碳酸钾、硝酸钾、氯化钾中的一种或几种物质组成,为探究其成分,某同学设计并完成了如图所示的实验.

根据以上实验,请你填空.
①由实验1可确定原营养液中一定没有的物质是
②若测得原营养液中K+、Cl-的数目之比为2:1,则原营养液是由
③某同学用氯化钙、硝酸钾、氯化钾配成的营养液中K+、Cl-、NO3-的数目之比为2:5:1,则所用硝酸钾和氯化钙的物质的量之比是
(2)下表是500mL某“鲜花保鲜剂”中含有的成分,阅读后回答下列问题.
| 成分 | 质量(g) | 摩尔质量(g?mol-1) |
| 蔗糖 | 68.4 | 342 |
| 硫酸钾 | 0.50 | 174 |
| 阿司匹林 | 0.35 | 180 |
| 高锰酸钾 | 0.50 | 158 |
| 硝酸银 | 0.04 | 170 |
②配制该500mL“鲜花保鲜剂”所需的玻璃仪器除了烧杯、玻璃棒、量筒外还有
③在溶液配制过程中,下列操作能使配制结果偏小的是
A.定容时仰视容量瓶刻度线
B.容量瓶在使用前未干燥,里面有少量蒸馏水
C.移液时,液体不小心从外壁流出
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理.
考点:探究物质的组成或测量物质的含量,配制一定物质的量浓度的溶液
专题:实验题
分析:(1)①根据硝酸钙、碳酸钾、硝酸钾、氯化钾几种物质中,硝酸钙可与碳酸钠生成白色碳酸钙沉淀进行解答;
②根据硝酸钙、硝酸钾、氯化钾几种物质中,氯化钾可与硝酸银生成白色氯化银沉淀,根据氯化钾溶液中钾离子与氯离子的个数比为1:1以及原营养液中K+、Cl-的数目之比为2:1进行解答;
③根据氯化钙、硝酸钾、氯化钾中含有的离子知识来回答.
(2)①根据物质的量浓度c=
来计算;
②根据配制一定物质的量浓度的溶液所需的仪器来回答;
③根据配制过程中溶质的物质的量以及溶液的体积两个方面来分析误差.
②根据硝酸钙、硝酸钾、氯化钾几种物质中,氯化钾可与硝酸银生成白色氯化银沉淀,根据氯化钾溶液中钾离子与氯离子的个数比为1:1以及原营养液中K+、Cl-的数目之比为2:1进行解答;
③根据氯化钙、硝酸钾、氯化钾中含有的离子知识来回答.
(2)①根据物质的量浓度c=
| n |
| V |
②根据配制一定物质的量浓度的溶液所需的仪器来回答;
③根据配制过程中溶质的物质的量以及溶液的体积两个方面来分析误差.
解答:
解:(1)①根据如图所示的实验1,向营养液中滴加碳酸钠溶液出现白色沉淀,可判断原营养液中一定含有硝酸钙;而硝酸钙与碳酸钾不能在同一溶液中共存,因此可判断原营养液中一定不含碳酸钾;硝酸钙可与碳酸钠生成白色碳酸钙沉淀,离子方程式是Ca2++CO32-=CaCO3↓;
故答案为:K2CO3;Ca2++CO32-=CaCO3↓;
②根据如图所示的实验2,向营养液中滴加硝酸银溶液出现白色沉淀,可判断营养液中一定含有氯化钾,氯化钾可与硝酸银生成白色氯化银沉淀,离子方程式是Ag++Cl-=AgCl↓;如果原营养液是硝酸钙与氯化钾的混合溶液,溶液中的钾离子与氯离子个数比只能为1:1,而测定结果营养液中钾离子与氯离子个数比为2:1,因此,原营养液中还应含有硝酸钾;综上所述,原营养液应是硝酸钙、氯化钾、硝酸钾三种物质的混合溶液;
故答案为:3;
③设氯化钙、硝酸钾、氯化钾的物质的量分别是x、y、z,K+、Cl-、NO3-的数目之比等于物质的量之比,即为2:5:1,则钾离子的物质的量为y+z,氯离子的物质的量为:2x+z,硝酸根离子的物质的量为y,则
=
,即y=z,则
=
=
,即x=2z,所以y:x=1:2,故答案为:1:2;
(2)①蔗糖的物质的量n=
=
=0.2mol,物质的量浓度c=
=
=0.4mol/L,故答案为:0.4mol/L;
②配制一定物质的量浓度的溶液所需的仪器:天平、烧杯、胶头滴管、玻璃棒、量筒、一定规格的容量瓶,故答案为:500mL的容量瓶、胶头滴管;
③A.定容时仰视容量瓶刻度线,会导致加水量多,体积偏大,浓度偏小,故A正确;
B.容量瓶在使用前未干燥,里面有少量蒸馏水,不影响实验结果,故B错误;
C.移液时,液体不小心从外壁流出会导致溶质的损失,则所配溶液的浓度偏小,故C正确;
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理是正确的,即对浓度无影响,故D错误;
故答案为:AC.
故答案为:K2CO3;Ca2++CO32-=CaCO3↓;
②根据如图所示的实验2,向营养液中滴加硝酸银溶液出现白色沉淀,可判断营养液中一定含有氯化钾,氯化钾可与硝酸银生成白色氯化银沉淀,离子方程式是Ag++Cl-=AgCl↓;如果原营养液是硝酸钙与氯化钾的混合溶液,溶液中的钾离子与氯离子个数比只能为1:1,而测定结果营养液中钾离子与氯离子个数比为2:1,因此,原营养液中还应含有硝酸钾;综上所述,原营养液应是硝酸钙、氯化钾、硝酸钾三种物质的混合溶液;
故答案为:3;
③设氯化钙、硝酸钾、氯化钾的物质的量分别是x、y、z,K+、Cl-、NO3-的数目之比等于物质的量之比,即为2:5:1,则钾离子的物质的量为y+z,氯离子的物质的量为:2x+z,硝酸根离子的物质的量为y,则
| y+z |
| y |
| 2 |
| 1 |
| 2x+z |
| y |
| 2x+z |
| z |
| 5 |
| 1 |
(2)①蔗糖的物质的量n=
| m |
| M |
| 68.4g |
| 342g/mol |
| n |
| V |
| 0.2mol |
| 0.5L |
②配制一定物质的量浓度的溶液所需的仪器:天平、烧杯、胶头滴管、玻璃棒、量筒、一定规格的容量瓶,故答案为:500mL的容量瓶、胶头滴管;
③A.定容时仰视容量瓶刻度线,会导致加水量多,体积偏大,浓度偏小,故A正确;
B.容量瓶在使用前未干燥,里面有少量蒸馏水,不影响实验结果,故B错误;
C.移液时,液体不小心从外壁流出会导致溶质的损失,则所配溶液的浓度偏小,故C正确;
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理是正确的,即对浓度无影响,故D错误;
故答案为:AC.
点评:本题考查了物质的推断及一定物质的量浓度溶液的配制过程中的计算和误差分析,(1)有一定难度,熟练掌握各种物质的溶解性是解答本类问题的关键,如常见的钾盐、钠盐、铵盐、硝酸盐都是可溶性盐,而氯化银、大多数的碳酸盐都不溶.

练习册系列答案
相关题目
下列离子方程式中书写正确的是( )
| A、FeCl2溶液中通入Cl2 Fe2++Cl2═Fe3++2Cl- |
| B、Al2O3与NaOH溶液反应 Al2O3+2OH-═2AlO2-+H2O |
| C、FeCl3溶液与铜 Fe3++Cu═Fe2++Cu2+ |
| D、用醋酸除水垢 2CH3COOH+CaCO3═2CH3COO-+Ca2++H2O+CO2 |
 在450℃并有催化剂存在下,于一容积恒定的密闭容器内进行下列反应:
在450℃并有催化剂存在下,于一容积恒定的密闭容器内进行下列反应: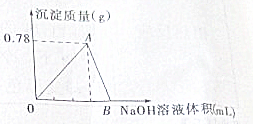 向20mL AlCl3溶液中滴入2mol?L-1 NaOH溶液时,沉淀质量与所滴加NaOH溶液体积(mL)关系如图所示:
向20mL AlCl3溶液中滴入2mol?L-1 NaOH溶液时,沉淀质量与所滴加NaOH溶液体积(mL)关系如图所示: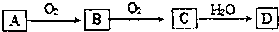
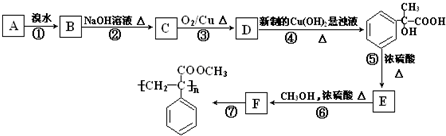
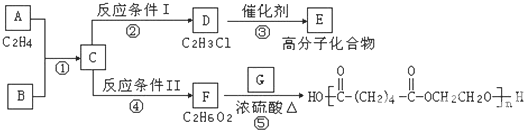
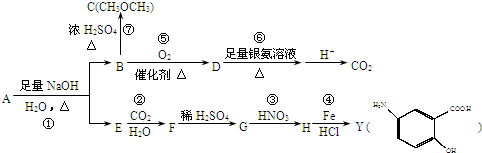

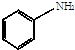
 和
和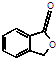 ,鉴别I和J的试剂为
,鉴别I和J的试剂为 )制得.请写出以L为原料制得M的合成路线流程图(无机试剂任用).流程图示例如下:
)制得.请写出以L为原料制得M的合成路线流程图(无机试剂任用).流程图示例如下: )→
)→