题目内容
3.下列措施能减慢化学反应速率的是( )| A. | 将煤块粉碎后燃烧 | |
| B. | 用2mol/L的盐酸代替1mol/L的盐酸制取氢气 | |
| C. | 将食物贮藏在冰箱中 | |
| D. | 用H2O2溶液制取氧气时加入少量二氧化锰粉末 |
分析 减慢反应速率,可降低温度、减小浓度或减小固体的表面积等,以此解答.
解答 解:A.固体的表面积增大,反应速率增大,故A错误;
B.用2mol/L的盐酸代替1mol/L的盐酸制取氢气,盐酸浓度增加,反应速率增大,故B错误.
C.食物储存在冰箱里,温度降低,反应速率减小,故C正确;
D.加入二氧化锰,起到催化剂作用,反应速率增大,故D错误;
故选C.
点评 本题考查反应速率的影响,为高频考点,侧重于基本理论的理解和应用的考查,注意相关基础知识的积累,难度不大.

练习册系列答案
相关题目
13.下列说法正确的是( )
| A. | 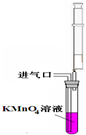 用如图所示装置测定空气中甲醛含量,若抽气速度过快会导致测定的甲醛含量偏低 | |
| B. | 溶质的溶解度越大,溶液的浓度越高,溶剂的蒸发速度越快,溶液的冷却速度越快,析出的晶体就越细小 | |
| C. | 将20g硝酸钠和17g氯化钾放入100ml烧杯中,加35mL水,并加热、搅拌,使溶液浓缩至约为原来的一半时,趁热过滤即可得到硝酸钾晶体 | |
| D. | 用移液管取液后,将移液管垂直伸入容器里面,松开食指使溶液全部流出,数秒后取出 |
14.环丙叉环丙烷(A)由于其特殊的电子结构,一直受到结构和理论化学家的注意,由于缺乏有效的合成途径,一度延缓对其反应的研究,直到1993年出现了可以大量制备的方法.根据下列转化,判断下列说法正确的是( )


| A. | A的所有原子都在一个平面内 | B. | 反应①是加成反应 | ||
| C. | 反应②是消去反应 | D. | A的二取代产物只有1种 |
11.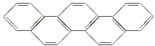 2016年夏季奥运会将在“足球王国”--巴西首都里约热内卢举行,如图酷似奥林匹克旗中的五环的一种有机物被称之为奥林匹克烃,下列说法正确的是( )
2016年夏季奥运会将在“足球王国”--巴西首都里约热内卢举行,如图酷似奥林匹克旗中的五环的一种有机物被称之为奥林匹克烃,下列说法正确的是( )
 2016年夏季奥运会将在“足球王国”--巴西首都里约热内卢举行,如图酷似奥林匹克旗中的五环的一种有机物被称之为奥林匹克烃,下列说法正确的是( )
2016年夏季奥运会将在“足球王国”--巴西首都里约热内卢举行,如图酷似奥林匹克旗中的五环的一种有机物被称之为奥林匹克烃,下列说法正确的是( )| A. | 该有机物属于芳香族化合物,是苯的同系物 | |
| B. | 该有机物中只含非极性键 | |
| C. | 该有机物的一氯代物有11种 | |
| D. | 该有机物完全燃烧生成H2O的物质的量小于CO2的物质的量 |
18.除去下列物质中的杂质(括号中为杂质),采用的试剂和除杂方法错误的是( )
| 选项 | 含杂质的物质 | 试剂 | 除杂方法 |
| A | C2H4(SO2) | NaOH溶液 | 洗气 |
| B | C6H6(苯酚) | 浓Br2水 | 过滤 |
| C | C6H5NO2(HNO3) | NaOH溶液 | 分液 |
| D | C2H2(H2S) | CuSO4溶液 | 洗气 |
| A. | A | B. | B | C. | C | D. | D |
8.下列离子方程式书写正确的是( )
| A. | AlCl3溶液中加入过量氨水:Al3++3NH3•H2O═Al(OH)3↓+3NH4+ | |
| B. | 用FeCl3溶液刻蚀铜电路板:Cu+Fe3+═Cu2++Fe2+ | |
| C. | 稀硝酸滴到大理石上:CO32-+2H+═H2O+CO2↑ | |
| D. | 铜和浓硝酸反应:Cu+4H++2NO3-═Cu2++2NO2↑+2H2O |
15.下列离子中,电子数大于质子数且质子数大于中子数的是( )
| A. | H3O+ | B. | Li+ | C. | OD- | D. | OH- |
12.用飞秒激光技术研究了氰化碘的分解反应:ICN→I+CN,发现该反应可在200飞秒内完成.己知(CN)2和卤素的性质相似.以下有关ICN的叙述正确的是( )
| A. | ICN不能和NaOH溶液作用 | |
| B. | ICN是一种离子化合物 | |
| C. | ICN可以和NaI作用生成单质碘 | |
| D. | ICN空气中受热也能发生题中所述分解反应 |
13.下列物质的转化在给定条件下能实现的是( )
| A. | NaCl(aq)$\stackrel{CO_{2}}{→}$NaHCO3(s) $\stackrel{△}{→}$Na2CO3(s) | |
| B. | CuCl2$\stackrel{NaOH(aq)}{→}$ Cu(OH)2 $→_{△}^{葡萄糖}$Cu | |
| C. | Al $\stackrel{NaOH(aq)}{→}$ NaAlO2(aq) $\stackrel{△}{→}$ NaAlO2(s) | |
| D. | MgO(s)$\stackrel{HNO_{3}(aq)}{→}$ Mg(NO3)2(aq) $\stackrel{电解}{→}$ Mg(s) |