题目内容
在下列试剂中,可以一次性将Ba(OH)2,HCl,NaCO3三种溶液区别开来的试剂的是( )
| A、稀硫酸 | B、氯化钡溶液 |
| C、硝酸银溶液 | D、稀硝酸 |
考点:物质的检验和鉴别的基本方法选择及应用
专题:物质检验鉴别题
分析:A、稀硫酸与Ba(OH)2混合产生沉淀,与碳酸钠混合有气体,与HCl不反应;
B、氯化钡溶液和氢氧化钡、HCl混合均无现象;
C、Ba(OH)2,HCl,NaCO3与硝酸银均生成沉淀;
D、稀硝酸与Ba(OH)2、HCl混合均无明显现象.
B、氯化钡溶液和氢氧化钡、HCl混合均无现象;
C、Ba(OH)2,HCl,NaCO3与硝酸银均生成沉淀;
D、稀硝酸与Ba(OH)2、HCl混合均无明显现象.
解答:
解:A、硫酸与氯化钠不反应,稀硫酸和氢氧化钡发生中和反应生成白色的硫酸钡沉淀,稀硫酸与碳酸钠反应生成无色气体,三种物质中的现象不同,可以鉴别,故A正确;
B、氯化钡溶液和氢氧化钡、HCl都不会反应,混合无现象,碳酸钠和氯化钡反应生成碳酸钡沉淀,不可以鉴别,故B错误;
C、硝酸银溶液与Ba(OH)2,HCl,NaCO3三种溶液均能产生沉淀,所以不能鉴别,故C错误;
D、稀硝酸与氢氧化钡反应无明显现象,稀硝酸与盐酸不反应,与碳酸钠反应生成二氧化碳气体,所以不能鉴别,故D错误.
故选A.
B、氯化钡溶液和氢氧化钡、HCl都不会反应,混合无现象,碳酸钠和氯化钡反应生成碳酸钡沉淀,不可以鉴别,故B错误;
C、硝酸银溶液与Ba(OH)2,HCl,NaCO3三种溶液均能产生沉淀,所以不能鉴别,故C错误;
D、稀硝酸与氢氧化钡反应无明显现象,稀硝酸与盐酸不反应,与碳酸钠反应生成二氧化碳气体,所以不能鉴别,故D错误.
故选A.
点评:本题考查了物质的鉴别,区别物质时利用性质差异,选取现象明显的变化进行区别,有些反应无明显的实验现象,不适合用来区别物质,题目难度不大.

练习册系列答案
相关题目
工业上用CO生产燃料甲醇.一定条件下发生反应:CO(g)+2H2(g)?CH3OH(g).图1表示反应中能量的变化;图2表示一定温度下,在体积为2L的密闭容器中加入4mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化图.下列说法不正确的是( )
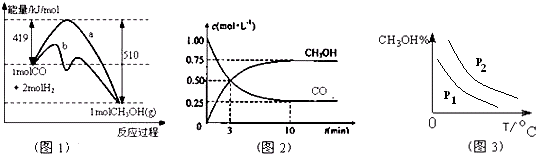

| A、曲线b表示使用了催化剂;该反应属于放热反应 |
| B、当压强不同时(P1<P2)时,平衡时甲醇百分含量(纵坐标)随温度(横坐标)变化的曲线如图3 |
| C、容器中压强恒定时,反应已达平衡状态 |
| D、该温度下CO(g)+2H2(g)?CH3OH(g)的化学平衡常数为10 |
向50g浓度为c mol?L-1,密度为ρg?cm-3的氨水中加入一定量的水,将其稀释至0.5c mol?L-1,则加入水的体积( )
| A、小于50mL | ||
| B、等于50mL | ||
| C、大于50mL | ||
D、等于
|
下列实验装置图正确的是( )
A、 实验室制乙烯 |
B、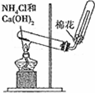 实验室制氨气 |
C、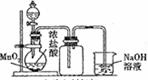 实验室制氯气 |
D、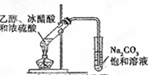 实验室制乙酸乙酯 |
设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A、标准状况下,0.1molCl2溶于水,转移的电子数目为0.1NA |
| B、标准状况下,11.2L甲醛气体中电子数为8NA |
| C、常温常压下,7.8g苯中含有单键的数目为0.6NA |
| D、1.0L0.1 mol?L-1 AlCl3溶液中所含的Al3+离子数为0.1NA |
下列判断或叙述正确的是( )
| A、某无色溶液中加入AgNO3溶液得白色沉淀,加稀硝酸沉淀不消失,则原液一定存在Cl- |
| B、某无色溶液中滴加BaCl2溶液得白色沉淀,加稀硝酸沉淀不溶解,则一定含有SO42- |
| C、提纯含有少量Ba(NO3)2杂质的KNO3,可加入过量的K2SO4溶液,过滤,再向滤液中滴加适量的稀硝酸 |
| D、某无色溶液中滴加入盐酸则生成无色气体,该气体能使澄清石灰水变浑浊,则原溶液中一定有CO32- |
下列说法不正确的是( )
| A、元素分析仪可同时对有机物中碳、氢、氧、硫等多种元素进行分析,其特点是样品量少,速度快 |
| B、1H核磁共振谱能反映出有机物中不同环境氢原子的种数和个数 |
| C、根据红外光谱图的分析可以初步判断有机物中具有哪些基团 |
| D、同位素示踪法可以用来确定有机反应中化学键的断裂位置 |
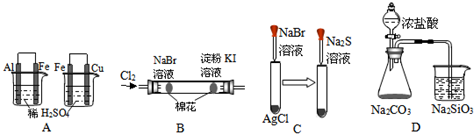
关于下列各装置图的叙述中,不正确的是( )
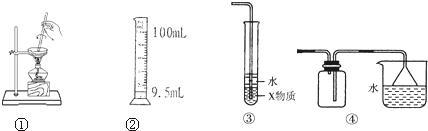

| A、装置①是把饱和食盐水中的食盐提取出来 |
| B、装置②用100mL量筒量取9.5mL液体 |
| C、装置③中X若为CCl4,可用于吸收NH3或HCl,并可防止倒吸 |
| D、装置④可用于收集NH3,并吸收多余的NH3 |