题目内容
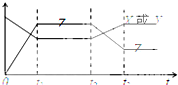
25℃时,由浓度均为1mol?L-1的弱酸(HA)及其盐(NaA)组成的混合溶液.往溶液中通入HCl气体或加入NaOH固体时,溶液pH随加入H+或OH-的物质的量而变化的曲线如图所示.下列说法中,正确的是( )

| A、加NaOH,HA电离平衡常数增大 |
| B、b点溶液中,c(HA)<c(A-) |
| C、溶液中水的电离程度a>b>c |
| D、通入HCl,溶液中阴离子浓度之和减小 |
考点:酸碱混合时的定性判断及有关ph的计算
专题:电离平衡与溶液的pH专题
分析:A.HA电离平衡常数与温度有关,与溶液的酸碱性无关;
B.b点时未加HCl和NaOH时,溶液呈酸性,说明HA的电离程度大于A-水解程度,据此判断c(HA)、c(A-)的浓度大小;
C.a、b溶液呈酸性,抑制水的电离,c呈中性,以此判断水的电离程度大小;
D.通入氯化氢,根据电荷守恒c(Cl-)+c(A-)+c(OH-)=c(Na+)+c(H+)可知,钠离子浓度基本不变、氢离子浓度增大,阴离子浓度则增大.
B.b点时未加HCl和NaOH时,溶液呈酸性,说明HA的电离程度大于A-水解程度,据此判断c(HA)、c(A-)的浓度大小;
C.a、b溶液呈酸性,抑制水的电离,c呈中性,以此判断水的电离程度大小;
D.通入氯化氢,根据电荷守恒c(Cl-)+c(A-)+c(OH-)=c(Na+)+c(H+)可知,钠离子浓度基本不变、氢离子浓度增大,阴离子浓度则增大.
解答:
解:A.电离平衡常数与温度应该,温度不变,电离平衡常数不变,所以加NaOH后,HA电离平衡常数不变,故A错误;
B.b点溶液中未加HCl和NaOH时,溶液呈酸性,c(OH-)<c(H+)说明HA的电离程度大于A-水解程度,则:c(A-)>c(HA),故B正确;
C.a、b溶液呈酸性,抑制水的电离,c呈中性,pH越小,酸性越强,水的电离程度越小,则a、b、c三点所表示的溶液中水的电离程度依次增大,即:a<b<c,故C错误;
D.通入氯化氢,氯化氢为强电解质,溶液酸性增强,即氢离子浓度增大,根据电荷守恒c(Cl-)+c(A-)+c(OH-)=c(Na+)+c(H+)可知,溶液中钠离子浓度基本不变,而氢离子浓度增大,则阴离子的总浓度增大,故D错误;
故选B.
B.b点溶液中未加HCl和NaOH时,溶液呈酸性,c(OH-)<c(H+)说明HA的电离程度大于A-水解程度,则:c(A-)>c(HA),故B正确;
C.a、b溶液呈酸性,抑制水的电离,c呈中性,pH越小,酸性越强,水的电离程度越小,则a、b、c三点所表示的溶液中水的电离程度依次增大,即:a<b<c,故C错误;
D.通入氯化氢,氯化氢为强电解质,溶液酸性增强,即氢离子浓度增大,根据电荷守恒c(Cl-)+c(A-)+c(OH-)=c(Na+)+c(H+)可知,溶液中钠离子浓度基本不变,而氢离子浓度增大,则阴离子的总浓度增大,故D错误;
故选B.
点评:本题考查酸碱混合的定性判断和计算,侧重于学生的分析能力和计算能力的考查,为高考常见题型和高频考点,注意把握图象所给信息,为解答该题的关键,难度中等.

练习册系列答案
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案
相关题目
 现有反应X(g)+Y(g)?2Z(g),△H<0.如图表示从反应开始到t1s时达到平衡,在t2s时由于条件变化使平衡破坏,到t3s时又达平衡,则在图中t2s时改变的条件可能是( )
现有反应X(g)+Y(g)?2Z(g),△H<0.如图表示从反应开始到t1s时达到平衡,在t2s时由于条件变化使平衡破坏,到t3s时又达平衡,则在图中t2s时改变的条件可能是( )| A、增大了X或Y的浓度 |
| B、增大压强 |
| C、增大Z的浓度 |
| D、升高温度 |
符合分子式C8H10的芳香烃的一氯代物同分异构体共有( )
| A、16种 | B、14种 |
| C、11种 | D、9种 |
下列除杂试剂或操作方法正确的一组是( )
| 序号 | 物质 | 杂质 | 除杂试剂或操作方法 |
| ① | KNO3溶液 | KOH | 加入FeCl3溶液,过滤 |
| ② | FeSO4溶液 | CuSO4 | 加入过量Fe粉,过滤 |
| ③ | H2 | CO2 | 通过盛NaOH溶液洗气瓶,再通过盛H2SO4洗气瓶 |
| ④ | NaNO3 | CaCO3 | 溶解,过滤,蒸发 |
| ⑤ | NaCl | KNO3 | 溶解,加热浓缩,冷却结晶,过滤 |
| A、②③④ | B、①②③④ |
| C、③④⑤ | D、②③⑤ |
下列关于化工生产原理的叙述中,符合目前工业生产实际的是( )
| A、氯碱工业中,离子交换膜的作用是防止离子运动 |
| B、硫酸、硝酸、合成氨均使用了催化剂 |
| C、石油裂化的主要目的是得到更多的乙烯、丙烯等气态短链烃 |
| D、氯气和氢气混合在光照条件下生成氯化氢,用水吸收得到盐酸 |
下列说法正确的是( )
| A、pH试纸使用时要先湿润试纸,再用玻璃棒蘸取待测液点试纸,半分钟内与比色卡对照 | ||
| B、pH=5的盐酸加水稀释1000倍后PH=8 | ||
| C、pH=6的溶液一定是酸性溶液 | ||
D、某溶液C(H+)=KW
|
下列关于干冰转化为二氧化碳气体的过程判断正确的是( )
| A、△H>0,△S<0 |
| B、△H<0,△S>0 |
| C、△H>0,△S>0 |
| D、△H<0,△S<0 |
下列表述中,合理的是( )
| A、用已知浓度的NaOH溶液测定盐酸的浓度,酸式滴定管未用待装溶液润洗会造成测定结果偏高 | ||||
B、Na2CO3溶液中:c(Na+)>c(CO
| ||||
| C、等体积等浓度的氢氧化钠与醋酸混合:c(Na+)=c(CH3COO-) | ||||
D、c(NH
|