题目内容
已知下列热化学方程式:
2H2(g)+O2(g)=2H2O(l)△H=-570kJ/mol,
H2(g)+
O2(g)=H2O(l)△H=-285.8kJ/mol,
H2(g)+
O2(g)=H2O(g)△H=-241.8kJ/mol,
C(g)+
O2(g)=CO (g)△H=-110.5KJ/mol,
回答下列各问题:
(1)H2的燃烧热△H=
(2)1mol液态水蒸发为气态水,需 (填“吸收”或“放出”)热量 kJ
(3)请写出C与水蒸气反应CO和H2的热化学方程式: .
2H2(g)+O2(g)=2H2O(l)△H=-570kJ/mol,
H2(g)+
| 1 |
| 2 |
H2(g)+
| 1 |
| 2 |
C(g)+
| 1 |
| 2 |
回答下列各问题:
(1)H2的燃烧热△H=
(2)1mol液态水蒸发为气态水,需
(3)请写出C与水蒸气反应CO和H2的热化学方程式:
考点:用盖斯定律进行有关反应热的计算,燃烧热
专题:化学反应中的能量变化
分析:(1)H2的燃烧热是指1mol氢气完全燃烧生成1mol液态水时放出的热量,燃烧热热化学方程式为H2(g)+
O2(g)=H2O(l)△H=-285.8kJ/mol;
(2)H2O(l)═H2O(g),汽化过程需要吸收热量,已知①H2(g)+
O2(g)=H2O(l)△H=-285.8kJ/mol,②H2(g)+
O2(g)=H2O(g)△H=-241.8kJ/mol,
由盖斯定律②-①得H2O(l)═H2O(g),△H=-241.8kJ/mol+285.8kJ/mol=+44kJ/mol;
(3)已知,②H2(g)+
O2(g)=H2O(g)△H=-241.8kJ/mol,③C(g)+
O2(g)=CO(g)△H=-110.5KJ/mol,由盖斯定律③-②得C(g)+H2O(g)=H2(g)+CO(g),△H=-110.5KJ/mol+241.8kJ/mol=131.3kJ/mol.
| 1 |
| 2 |
(2)H2O(l)═H2O(g),汽化过程需要吸收热量,已知①H2(g)+
| 1 |
| 2 |
| 1 |
| 2 |
由盖斯定律②-①得H2O(l)═H2O(g),△H=-241.8kJ/mol+285.8kJ/mol=+44kJ/mol;
(3)已知,②H2(g)+
| 1 |
| 2 |
| 1 |
| 2 |
解答:
解:(1)H2的燃烧热是指1mol氢气完全燃烧生成1mol液态水时放出的热量,燃烧热热化学方程式为H2(g)+
O2(g)=H2O(l)△H=-285.8kJ/mol,因此H2的燃烧热△H=-285.8kJ/mol,
故答案为:-285.8kJ/mol;
(2)H2O(l)═H2O(g),汽化过程需要吸收热量,已知①H2(g)+
O2(g)=H2O(l)△H=-285.8kJ/mol,②H2(g)+
O2(g)=H2O(g)△H=-241.8kJ/mol,
由盖斯定律②-①得H2O(l)═H2O(g),△H=-241.8kJ/mol+285.8kJ/mol=+44kJ/mol,
故答案为:吸收;44;
(3)已知,②H2(g)+
O2(g)=H2O(g)△H=-241.8kJ/mol,③C(g)+
O2(g)=CO(g)△H=-110.5KJ/mol,由盖斯定律③-②得C(g)+H2O(g)=H2(g)+CO(g),△H=-110.5KJ/mol+241.8kJ/mol=+131.3kJ/mol,
故答案为:C(g)+H2O(g)=H2(g)+CO(g)△H=+131.3kJ/mol.
| 1 |
| 2 |
故答案为:-285.8kJ/mol;
(2)H2O(l)═H2O(g),汽化过程需要吸收热量,已知①H2(g)+
| 1 |
| 2 |
| 1 |
| 2 |
由盖斯定律②-①得H2O(l)═H2O(g),△H=-241.8kJ/mol+285.8kJ/mol=+44kJ/mol,
故答案为:吸收;44;
(3)已知,②H2(g)+
| 1 |
| 2 |
| 1 |
| 2 |
故答案为:C(g)+H2O(g)=H2(g)+CO(g)△H=+131.3kJ/mol.
点评:本题考查了燃烧热、盖斯定律应用,根据题给方程式进行整合得出目标方程式,反应热进行相应的加合,难度不大.

练习册系列答案
相关题目
下列关于实验现象的描述不正确的是( )
| A、把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面出现气泡 |
| B、用铜片做阳极,铁片做阴极,电解氯化铜溶液,铁片表面出现一层铜 |
| C、用铜作阳极,电解FeCl3溶液,在阴极上可析出铜 |
| D、把锌粒放入盛有盐酸的试管中,加入几滴氯化铜溶液,气泡放出速率加快 |
下列叙述中正确的是( )
| A、(CH3)2C═CHCH2CH3分子中的六个碳原子中至少有五个在同一个平面上 |
| B、液化石油气和天然气的主要成分都是甲烷 |
| C、乙醇、丙三醇互为同系物,同系物之间不可能互为同分异构体 |
| D、间二溴苯仅有一种空间结构,这可以证明苯分子中不存在单双键交替的结构 |
 向100mL 0.1mol?L-1硫酸铝铵[NH4Al(SO4)2]溶液中逐滴滴入0.1mol?L-1 Ba(OH)2溶液.随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如图所示.则下列说法中正确的是( )
向100mL 0.1mol?L-1硫酸铝铵[NH4Al(SO4)2]溶液中逐滴滴入0.1mol?L-1 Ba(OH)2溶液.随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如图所示.则下列说法中正确的是( )| A、a点对应的沉淀只有BaSO4 |
| B、c点溶液铝元素以AlO2- 的形式存在 |
| C、b点发生反应的离子方程式是:Al3++2SO42-+2Ba2++3OH-=Al(OH)3↓+2BaSO4↓ |
| D、c点加入Ba(OH)2溶液的体积为200 mL |
以下涉及H2O2的反应(未配平)中,H2O2仅表现出氧化性的是( )
| A、Ag2O+H2O2═Ag+O2↑+H2O |
| B、H2O2═H2O+O2↑ |
| C、H2O2+Cr2(SO4)3+KOH═K2CrO4+K2SO4+H2O |
| D、Na2O2+HCl═H2O2+NaCl |
把一小块钠投入到滴有石蕊试液的水中,下列有关该实验现象的描述错误的是( )
| A、溶液变为红色 |
| B、可以听到“嘶嘶”的响声 |
| C、钠熔化成闪亮的小球 |
| D、钠在水面上四处游动 |
用NA表示阿伏加德罗常数的值.下列叙述中不正确的是( )
| A、分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA |
| B、28 g乙烯和环丁烷(C4H8)的混合气体中含有的碳原子数为2 NA |
| C、常温常压下,22.4L氯气与足量镁粉充分反应,转移的电子数为2 NA |
| D、常温常压下,92 g的NO2和N2O4混合气体含有的原子数为6 NA |
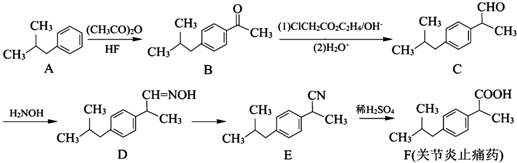
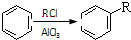 ②
②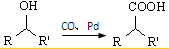 (R、R′表示烃基)
(R、R′表示烃基)