题目内容
将2.44g BaCl2?xH2O晶体溶于水中配成100mL溶液,将此溶液与200mL 0.1mol/L AgNO3溶液反应,恰好使Cl-完全反应.求:
(1)BaCl2?xH2O的摩尔质量;
(2)x的值;
(3)溶液中Ba2+的物质的量浓度.
(1)BaCl2?xH2O的摩尔质量;
(2)x的值;
(3)溶液中Ba2+的物质的量浓度.
考点:化学方程式的有关计算
专题:计算题
分析:(1)根据n=cV计算n(AgNO3),由题意知n(Cl-)=n(Ag+),进而计算n(BaCl2?xH2O),再根据M=
计算BaCl2?xH2O的摩尔质量;
(2)根据BaCl2?xH2O的相对分子质量计算x的值;
(3)n(Ba2+)=n(BaCl2?xH2O),根据c=
计算溶液中Ba2+的物质的量浓度.
| m |
| n |
(2)根据BaCl2?xH2O的相对分子质量计算x的值;
(3)n(Ba2+)=n(BaCl2?xH2O),根据c=
| n |
| V |
解答:
解:(1)n(AgNO3)=c(AgNO3)?V(溶液)=0.1mol/L×0.2L=0.02mol,
由题意可知,n(Cl-)=n(Ag+)=0.02mol,则n(BaCl2?xH2O)=
=0.01mol,
故M(BaCl2?xH2O)=
=244g/mol,
答:BaCl2?xH2O的摩尔质量为244g/mol.
(2)BaCl2?xH2O的相对分子质量为244,则:(137+71)+18x=244,解得x=2,
答:x的值为2.
(3)n(Ba2+)=n(BaCl2?xH2O)=0.01mol,则c(Ba2+)=
=0.1mol/L,
答:溶液中Ba2+的物质的量浓度为0.1mol/L.
由题意可知,n(Cl-)=n(Ag+)=0.02mol,则n(BaCl2?xH2O)=
| 0.02mol |
| 2 |
故M(BaCl2?xH2O)=
| 2.44g |
| 0.01mol |
答:BaCl2?xH2O的摩尔质量为244g/mol.
(2)BaCl2?xH2O的相对分子质量为244,则:(137+71)+18x=244,解得x=2,
答:x的值为2.
(3)n(Ba2+)=n(BaCl2?xH2O)=0.01mol,则c(Ba2+)=
| 0.01mol |
| 0.1L |
答:溶液中Ba2+的物质的量浓度为0.1mol/L.
点评:本题考查化学方程式有关计算,难度不大,明确发生的反应是解题关键,侧重对基础知识的巩固.

练习册系列答案
 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案
相关题目
a克铁粉与含有硫酸的硫酸铜溶液完全反应后,得到a克铜,则参加反应的硫酸铜与硫酸的物质的量之比是( )
| A、1:7 | B、7:1 |
| C、7:8 | D、8:7 |
下列电离方程式错误的是( )
| A、CaCl2=Ca2++2Cl- |
| B、NaHSO4=Na++H++SO42- |
| C、H2CO3=2H++CO32- |
| D、HNO3=H++NO3- |
将下列各种液体分别与溴水混合并振荡.不能发生反应,静置后溶液分层,且溴水层几乎无色的是( )
| A、裂化汽油 | B、酒精 | C、己烷 | D、苯 |
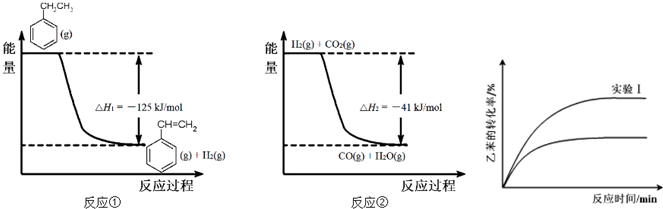
 (g)+CO2(g)?
(g)+CO2(g)? (g)+CO(g)+H2O(g)的△H=
(g)+CO(g)+H2O(g)的△H= )的影响,并设计了如下实验:
)的影响,并设计了如下实验: