题目内容
在水中加入等物质的量的MgSO4、NaCl、AgNO3三种物质组成混合溶液,该溶液在惰性材料作电极的电解槽中通电一段时间后,在两个电极区析出的氧化产物与还原产物的质量之比约为( )
| A、35.5:108 |
| B、16:207 |
| C、8:1 |
| D、108:35.5 |
考点:电解原理
专题:
分析:将等物质的量的MgSO4、NaCl、AgNO3混合均匀后,置于指定容器中,加入足量的水,发生反应:
AgNO3+NaCl=AgCl↓+NaNO3,反应后为MgSO4和NaNO3溶液,用铂电极电解,实际上电解的为水,在两极上分别生成氧气和氢气.
AgNO3+NaCl=AgCl↓+NaNO3,反应后为MgSO4和NaNO3溶液,用铂电极电解,实际上电解的为水,在两极上分别生成氧气和氢气.
解答:
解:将等物质的量的MgSO4、NaCl、AgNO3混合均匀后,置于指定容器中,加入足量的水,发生反应:
AgNO3+NaCl=AgCl↓+NaNO3,反应后为MgSO4和NaNO3溶液,
电解时发生:2H2O
2H2↑+O2↑,氧化产物为O2,还原产物为H2,
两极区析出的氧化产物与还原产物的质量比约为32:2×2=8:1,
故选C.
AgNO3+NaCl=AgCl↓+NaNO3,反应后为MgSO4和NaNO3溶液,
电解时发生:2H2O
| ||
两极区析出的氧化产物与还原产物的质量比约为32:2×2=8:1,
故选C.
点评:本题考查电解知识,题目难度中等,解答本题的关键是根据混合物的性质判断反应后滤液的成分,注意仔细审题.

练习册系列答案
 轻松暑假总复习系列答案
轻松暑假总复习系列答案
相关题目
向下列物质的溶液中通入过量的SO2,最终没有沉淀生成的是( )
| A、Na2S |
| B、Ca(OH)2 |
| C、Ca(NO3)2 |
| D、Ca(ClO)2 |
下列反应的离子方程式错误的是( )
| A、磷酸与氢氧化钾溶液反应:H++OH-=H2O |
| B、澄清石灰水跟稀硝酸反应:H++OH-=H2O |
| C、醋酸铵和盐酸反应:CH3COO-+H+=CH3COOH |
| D、碳酸钙溶于硝酸中:CaCO3+2H+=Ca2++H2O+CO2↑ |
将AlCl3、FeCl2、FeCl3、MgCl2四种溶液,只用一种试剂就能加以区别,这种试剂是( )
| A、HCl |
| B、NaOH |
| C、BaCl2 |
| D、KSCN |
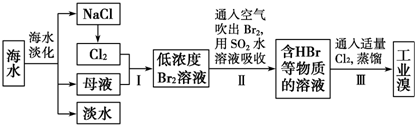
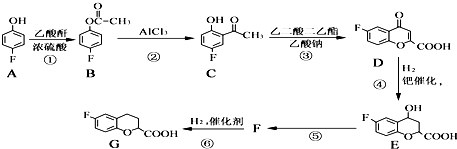
 请回答下列问题:
请回答下列问题: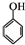 和乙酸酐为原料制备
和乙酸酐为原料制备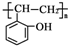 的合成路
的合成路