题目内容
19.向100mL的FeBr2溶液中通人标准状况下的Cl23.36L,反应后的溶液中Cl-和Br-的物质的量浓度相等,则原FeBr2溶液的物质的量浓度为2mol/L.分析 还原性Fe2+>Br-,通入氯气先发生反应2Fe2++Cl2═2Fe3++2Cl-,Fe2+反应完毕,剩余的氯气再发生反应2Br-+Cl2═Br2+2Cl-,反应后溶液中Cl-和Br-的物质的量浓度相等,说明氯气完全反应,Cl2的物质的量=$\frac{3.36L}{22.4L/mol}$=0.15mol,若Br-没有反应,溶液中n(Br-)=0.3mol,则n(FeBr2)=0.15mol,0.15molFe2+只能消耗0.075mol的Cl2,故有部分Br-参加反应,设FeBr2的物质的量为x,表示出参加反应的n(Br-),根据电子转移守恒列方程计算x值,再根据c=$\frac{n}{V}$计算.
解答 解:还原性Fe2+>Br-,通入氯气先发生反应2Fe2++Cl2═2Fe3++2Cl-,Fe2+反应完毕,剩余的氯气再发生反应2Br-+Cl2═Br2+2Cl-,反应后溶液中Cl-和Br- 的物质的量浓度相等,说明氯气完全反应,Cl2的物质的量=$\frac{3.36L}{22.4L/mol}$=0.15mol,若Br-没有反应,n(Br-)=0.3mol,则n(FeBr2)=0.15mol,0.15molFe2+只能消耗0.075mol的Cl2,故有部分Br-参加反应,
设FeBr2的物质的量为x,则n(Fe2+)=x mol,n(Br-)=2x mol,未反应的n(Br-)=0.3 mol,参加反应的n(Br-)=(2x-0.3)mol,根据电子转移守恒有x×1+[2x-0.3]×1=0.15mol×2,解得x=0.2 mol,所以原FeBr2溶液的物质的量浓度为$\frac{0.2mol}{0.1L}$=2mol/L.
故答案为:2mol/L.
点评 本题考查反应方程式的计算,侧重考查学生的分析、计算能力,难度中等,判断Br-是否完全反应是解题的关键,注意还原性Fe2+>Br-,通入的Cl2后发生反应有先后顺序.

 名校课堂系列答案
名校课堂系列答案| A. | 热能要充分利用 | |
| B. | 充足的空气就是指空气的量越大越好 | |
| C. | 固体燃料燃烧前要粉碎 | |
| D. | 液体燃料燃烧时可以雾状喷出 |
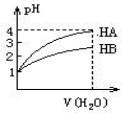 常温时,pH=1的两种一元酸HA和HB溶液,分别加水稀释1000倍,两溶液的pH与所加水的体积变化如图所示,下列结论中正确的是( )
常温时,pH=1的两种一元酸HA和HB溶液,分别加水稀释1000倍,两溶液的pH与所加水的体积变化如图所示,下列结论中正确的是( )| A. | 在稀释过程中当两者pH分别都是2时,c(HA)>c(HB) | |
| B. | 当稀释100倍时,HB溶液的pH=2 | |
| C. | 在稀释过程中HA与HB溶液中c(OH-)均增大 | |
| D. | 等体积pH=1的HA和HB溶液分别用等物质的量浓度的NaOH溶液中和,消耗碱溶液体积HA等于HB |
| A. | pH=2 的HA溶液与pH=12的MOH溶液等体积混合:c(H+)=c(OH-) | |
| B. | pH相等的CH3COONa、NaOH和Na2CO3三种溶液:c(NaOH)<c(CH3COONa)<c(Na2CO3) | |
| C. | 物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合:c(CH3COO-)+2c(OH-)=2c(H+)+c(CH3COOH) | |
| D. | 0.1mol•L-1的NaHA溶液,其pH=4:c(HA-)>c(H+)>c(H2A)>c(A2-) |
| 选项 | 实验目的 | 实验方案 |
| ① | 检验淀粉是否水解生成葡萄糖 | 向淀粉溶液中加入稀H2SO4,加热几分钟,冷却后水解液用NaOH溶液中和,然后再加入新制Cu(OH)2浊液,加热,观察是否有红色沉淀生成 |
| ② | 比较H2CO3、HCN的酸性强弱 | 用pH计测定同温度同浓度的Na2CO3溶液和NaCN溶液 的pH值,比较pH大小 |
| ③ | 区别植物油和矿物油 | 向植物油和矿物油中分别加入烧碱溶液,加热,冷却后观察是否分层 |
| ④ | 验证CaCO3的溶解度小于CaSO4 | 将浓Na2CO3溶液加入CaSO4悬浊液中,充分振荡,过滤、洗涤,向所得固体中滴加盐酸,观察是否有气体生成 |
| A. | ①② | B. | ②③ | C. | ③④ | D. | ①③ |
| A. | 增大压强.V正增大,V逆减小 | |
| B. | 升高温度,V正减小,V逆增大 | |
| C. | 增大A浓度的瞬间,V正增大,V逆不变 | |
| D. | 增大A浓度瞬间,V正增大而V逆减小 |
| A. | 煤的干馏 | B. | 石油的分馏 | C. | 石油的催化裂化 | D. | 煤的液化 |