题目内容
4.室温下,H2+Cl2$\stackrel{点燃}{→}$2HCl生成0.1molHCl,下列说法不正确的是( )| A. | 生成0.1NA根共价键 | B. | 消耗反应物总体积2.24L | ||
| C. | 转移了2NA个电子 | D. | 产物溶于水后,溶液pH=1 |
分析 A.HCl的结构简式为H-Cl,则NA个HCl中含NA根共共价键;
B.据H2+Cl2$\stackrel{点燃}{→}$2HCl此方程式中盐酸的量,求消耗反应的总体积;
C.据H2+Cl2$\stackrel{点燃}{→}$2HCl~2NA,此方程式中盐酸的量,求转移电子数;
D.pH=-lgc(H+),据此进行计算;
解答 解:A.HCl的结构简式为H-Cl,则NA个HCl中含NA根共共价键,故0.1mol即0.1NA个HCl中含0.1NA根共共价键,故A正确;
B.H2+Cl2$\stackrel{点燃}{→}$2HCl~反应物总体积44.8L
2 44.8
0.1 2.24L,故B正确;
C.H2+Cl2$\stackrel{点燃}{→}$2HCl~2NA
2 2NA
0.1 0.1NA,故C错误;
D.pH=-lgc(H+)=-lg0.1=1,故D正确,
故选C.
点评 本题考查氧化还原反应计算,D选项为易错点,学生容易忽略pH的计算公式,本题难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
14.下列各组中的物质均能发生加成反应的是( )
| A. | 乙烯和乙醇 | B. | 苯和乙醛 | C. | 乙酸和氯乙烯 | D. | 丙醛和丙烷 |
15.25℃时,0.1mol•L-1CH3COONa溶液的pH=a,下列说法错误的是( )
| A. | 该溶液中由水电离出的c(OH-)=10a-14 | |
| B. | 加水稀释,$\frac{c(C{H}_{3}COOH)}{c(C{H}_{3}CO{O}^{-})•c({H}^{+})}$减小 | |
| C. | 该温度下,pH=a的NaOH溶液的物质的量浓度小于0.1mol•L-1 | |
| D. | 加入等浓度、等体积的CH3COOH溶液,所得溶液中c(CH3COO-)+c(CH3COOH)=2c(Na+) |
19.下列关于价电子排布为3s23p4的原子描述正确的是( )
| A. | 它的元素符号为O | |
| B. | 它的核外电子排布式为1s22s22p63s23p4 | |
| C. | 可以与H2化合生成液态化合物 | |
| D. | 其电子排布图为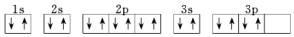 |
 (1)完全燃烧0.1mol某烃,燃烧产物依次通过浓硫酸、浓碱液,实验结束后,称得浓硫酸增重9g,浓碱液增重17.6g.该烃的化学式C4H10,并写出其所有可能的结构简式:CH3CH2CH2CH3、CH3CH(CH3)CH3.
(1)完全燃烧0.1mol某烃,燃烧产物依次通过浓硫酸、浓碱液,实验结束后,称得浓硫酸增重9g,浓碱液增重17.6g.该烃的化学式C4H10,并写出其所有可能的结构简式:CH3CH2CH2CH3、CH3CH(CH3)CH3.