��Ŀ����
3����֪Br2+2Fe2+�T2Br -+2Fe3+����������a mol��FeBr2��Һ��ͨ��b mol Cl2����ַ�Ӧ������˵������ȷ���ǣ�������| A�� | ���ӵĻ�ԭ��ǿ����Fe2+��Br-��Cl- | |
| B�� | ����������ʱ�����������ӷ�Ӧ��2Fe2++Cl2�T2Fe3++2Cl- | |
| C�� | ��a=bʱ����Ӧ����Һ������Ũ�ȣ�c��Fe3+����c��Br-����c��Cl-��=1��2��2 | |
| D�� | ����������ʱ���������ӷ�Ӧ��2Fe2++4Br-+3Cl2�T2Fe3++2Br2+6Cl- |
���� ��ԭ��Fe2+��Br-�����ȷ�����Ӧ��2Fe2++Cl2=2Fe3++2Cl-��Fe2+��Ӧ��ϣ��ٷ�����Ӧ��2Br-+Cl2=2Cl-+Br2��a mol��FeBr2��Һ�к���amolFe2+��2amolBr-��
A��������Խǿ����Ӧ���ӵĻ�ԭ��Խ����
B����������ʱ��ֻ���������ӱ�������
C����a=bʱ����2Fe2++Cl2=2Fe3++2Cl-��֪��amolFe2+����0.5amolCl2������amolFe3+��amolCl-����2Br-+Cl2=2Cl-+Br2��֪��0.5amolCl2������amolBr-��������amolCl-����Һ��ʣ��Br-Ϊamol��
D����������ʱ���������Ӻ������Ӷ���ȫ��������
��� �⣺��ԭ��Fe2+��Br-�����ȷ�����Ӧ��2Fe2++Cl2=2Fe3++2Cl-��Fe2+��Ӧ��ϣ��ٷ�����Ӧ��2Br-+Cl2=2Cl-+Br2��a mol��FeBr2��Һ�к���amolFe2+��2amolBr-��
A��������Խǿ����Ӧ���ӵĻ�ԭ��Խ���������ӵĻ�ԭ��ǿ����Fe2+��Br-��Cl-����A��ȷ��
B������������ʱ��ֻ��Fe2+��������������Ӧ���ӷ���ʽΪ��2Fe2++Cl2=2Fe3++2Cl-����B��ȷ��
C����a=bʱ����2Fe2++Cl2=2Fe3++2Cl-��֪��amolFe2+����0.5amolCl2������amolFe3+��amolCl-����2Br-+Cl2=2Cl-+Br2��֪��0.5amolCl2������amolBr-��������amolCl-����Һ��ʣ��Br-Ϊamol����Ӧ�������Ũ�ȣ�c��Fe3+����c��Br-����c��Cl-��=a��a��2a=1��1��2����C����
D����������ʱ���������Ӻ������Ӷ���ȫ���������������ӷ�ӦΪ��2Fe2++4Br-+3Cl2�T2Fe3++2Br2+6Cl-����D��ȷ��
��ѡC��
���� ���⿼��������ԭ��Ӧ���㡢���ӷ���ʽ��д�ȣ���Ŀ�Ѷ��еȣ��ؼ�����ȷ���ӷ�����Ӧ���Ⱥ�˳������������ѧ���ķ������������Ӧ��������

| A�� | Cl2��H2O��Ӧ��Cl2+H2O�T2H++Cl-+ClO- | |
| B�� | Fe��ϡ���ᷴӦ��Fe+2H+�TFe3++H2�� | |
| C�� | ��ˮ��FeCl3��Һ��Ӧ��3OH-+Fe3+�TFe��OH��3�� | |
| D�� | NaOH�����ᷴӦ��OH-+H+�TH2O |
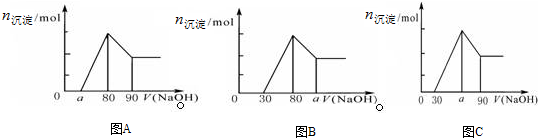
| A�� | Aͼ��a��ȡֵ��ΧΪ 0��a��50 | |
| B�� | Aͼ��$\frac{n��Mg��}{n��Al��}$�����ֵΪ2.5 | |
| C�� | ������ϵͼ��ΪBͼʱ����a��ȡֵ��ΧΪ80��a��90 | |
| D�� | ������ϵͼ��ΪCͼʱ����a��ȡֵ��ΧΪ75��a��90 |
| A�� | ��ҵ�ɲ��û���ͭ��Cu2S+O2�T2Cu+SO2 ÿ����2molͭ����Ӧ��ת��6NA������ | |
| B�� | ��״���£�11.2L�ױ����еķ�����Ϊ0.5NA | |
| C�� | 20g��ˮ��D2O�������ĵ�����Ϊ10NA | |
| D�� | 60gSiO2�й��õ��Ӷ���ĿΪ4NA |
| A�� | KOH��Һ | B�� | K2SO4��Һ | C�� | K2CO3��Һ | D�� | ������Һ |
 ��
��
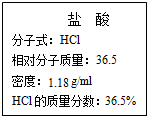 ��ͼΪʵ����ijŨ�����Լ�ƿ��ǩ�ϵ��й����ݣ��Ը��ݱ�ǩ�ϵ��й����ݻش��������⣺
��ͼΪʵ����ijŨ�����Լ�ƿ��ǩ�ϵ��й����ݣ��Ը��ݱ�ǩ�ϵ��й����ݻش��������⣺