题目内容
13.实验室需要0.1mol•L-1 NaOH溶液450mL和0.5mol•L-1硫酸溶液350mL.根据这两种溶液的配制情况回答下列问题:(1)配制上述溶液需用到的玻璃仪器是量筒、玻璃棒、烧杯、500mL容量瓶、胶头滴管(填仪器名称).
(2)下列操作中,容量瓶所不具备的功能有BCD(填序号).
A.配制一定体积准确浓度的标准溶液
B.贮存溶液
C.测量容量瓶规格以下的任意体积的液体
D.准确稀释某一浓度的溶液
E.用来加热溶解固体溶质
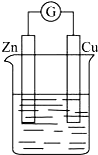
(3)请计算需用托盘天平称取固体NaOH的质量为2.0g,某同学用托盘天平称量烧杯的质量,天平平衡后的状态如图.由图中可以看出,烧杯的实际质量为27.4 g.

(4)根据计算得知,用量筒量取所需质量分数为98%、密度为1.84g•cm-3的浓硫酸的体积为13.6mL.若将原浓硫酸与等体积的水混合,所得溶液中溶质的质量分数>49%(填“<”、“=”或“>”);若将原硫酸与等质量的水混合,所得溶液的物质的量浓度<9.2mol•L-1.
分析 (1)依据配制一定物质的量浓度溶液的一般步骤,选择需要的仪器;
(2)容量瓶不能稀释浓溶液、不能用于溶解固体、储存溶液等;
(3)依据m=CVM计算需要溶质的质量;根据左码右物称量药品时,药品的实际质量=砝码的质量-游码的质量,精确值为0.1g;
(4)根据c=$\frac{1000ρω}{M}$计算出该浓硫酸的物质的量浓度,再根据配制过程中溶质硫酸的物质的量不变计算出需要浓硫酸的体积;
硫酸与水的密度不同,水分子与硫酸分子间有间隙,等体积混合,混合所得溶液的总体积小于硫酸体积的二倍;
硫酸的浓度越大密度越大,该硫酸与等质量的水混合,质量变为2倍,密度降低,体积比原浓硫酸的2倍大,结合稀释定律判断.
解答 解:(1)配制一定物质的量浓度溶液的一般步骤:计算、称量(量取)、溶解(稀释)、冷却、移液、洗涤、定容、摇匀,用到的仪器:托盘天平、药匙、量筒、烧杯、玻璃棒、500mL容量瓶、胶头滴管,所以还缺少的仪器:500mL容量瓶、胶头滴管;
故答案为:500mL容量瓶、胶头滴管;
(2)容量瓶只能用来配制一定体积准确浓度的溶液,不能配制或测量容量瓶规格以下的任意体积的液体,不能稀释或溶解药品,不能用来加热溶解固体溶质,
故选BCD;
(3)需要0.1mol•L-1 NaOH溶液450mL,应选择500mL容量瓶,需要溶质的质量m=0.1mol/L×40g/mol×
0.5L=2.0g;
图中物质和砝码的位置放反了,质量关系应为:砝码的质量=烧杯的质量+游码显示的质量.即30 g=烧杯的质量+2.6 g,得烧杯的质量为:30g-2.6g=27.4g.
故答案为:2.0;27.4;
(4)分数为98%、密度为1.84g•cm-3的浓硫酸的浓度为:c=$\frac{1000×1.84×98%}{98}$mol/L=18.4mol/L,
设需要浓硫酸体积为V,则V×18.4mol/L=0.5mol/L×500mL,解得V=13.6mL;
硫酸与等体积水混合后,所得溶液中硫酸的物质的量不变,则稀释前后,硫酸的物质的量不变,C1V1=C2V2,所以C2=$\frac{{C}_{1}{V}_{1}}{{V}_{2}}$=$\frac{18.4{V}_{1}}{{V}_{2}}$,但是V2<2V1,所以所得溶液的物质的量浓度大于9.2mol/L;
硫酸的浓度越大密度越大,该硫酸与等质量的水混合,质量变为2倍,密度降低,体积比原浓硫酸的2倍大,根据稀释定律,稀释前后溶质硫酸的物质的量不变,所以浓度小于原浓硫酸的$\frac{1}{2}$,混合所得溶液的物质的量浓度小于9.2 mol/L;
故答案为:13.6;>;<;
点评 本题考查了一定物质的量浓度溶液的配制及有关物质的量计算,明确配制原理及硫酸溶液的密度与浓度的关系是解题关键,题目难度中等.

 名校课堂系列答案
名校课堂系列答案| A. | 只滴加氨水鉴别NaCl、AlCl3、MgCl2、Na2SO4四种溶液 | |
| B. | 用澄清石灰水鉴别Na2CO3、NaHCO3两种溶液 | |
| C. | 用萃取分液的方法除去酒精中的水 | |
| D. | 用可见光束照射以区别溶液和胶体 |
| 应称量NaOH的质量/g | 应选用容量瓶的规格/mL | 除容量瓶外还需要的其它仪器 |
| 4.0 | 500 | 烧杯、量筒、玻璃棒、药匙、托盘天平、胶头滴管 |
A.所用NaOH已经潮解
B.向容量瓶中加水未到刻度线
C.有少量NaOH溶液残留在烧杯里
D.称量时误用“左码右物”
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
(1)某小组用NaCl进行以下实验:
| 步 骤 | 现 象 |
| Ⅰ.将NaCl溶液与AgNO3溶液混合 | 产生白色沉淀 |
| Ⅱ.向所得固液混合物中加Na2S溶液 | 沉淀变为黑色 |
| Ⅲ.将Ⅱ中经过滤洗得到的黑色沉淀分成两份,在一份沉淀中加蒸馏水,另一份沉淀中加入NaCl溶液,同时浸泡较长时间. | 加蒸馏水的沉淀仍为黑色,加入NaCl溶液的沉淀变为乳白色 |
②Ⅱ中能说明沉淀变黑的离子方程式是2AgCl(s)+S2-(aq)=Ag2S(s)+2Cl-,沉淀能发生转化的主要原因是Ag2S比AgCl溶解度更小.
③经检测步骤Ⅲ中乳白色沉淀是AgCl和S的混合物.请写出黑色沉淀变为乳白色的化学方程式2Ag2S+O2+4NaCl+2H2O=4AgCl+2S+4NaOH,从化学平衡移动的角度解释在沉淀变色过程中NaCl的作用Ag2S被O2氧化生成S时释放出Ag+,NaCl中的Cl-与Ag+结合成AgCl沉淀,c(Ag+)减小,③中平衡向正反应方向移动,最终出现乳白色沉淀.
(2)电解法是治理铵盐为主要水体污染物的一种方法,原理是:在污水中加入一定量NaCl进行电解,产生的Cl2与水反应生成HClO,HClO 将NH4+氧化为N2,使水体脱氮.请写出酸性条件下HClO 与NH4+反应的离子方程式3HClO+2NH4+=N2↑+3Cl-+5H++3H2O.研究发现:污水呈弱酸性比强酸性更有利于使NH4+氧化为N2而脱氮,原因是酸性较强时,Cl2+H2O?H++Cl-+HClO 的化学平衡向逆反应方向移动,生成的HClO减少,不利脱氮.

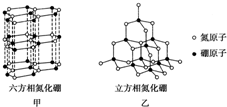 氮化硼(BN)晶体有多种相结构.六方相氮化硼是通常存在的稳定相,与石墨相似,只有层状结构,可作高温润滑剂.立方相氮化硼是超硬材料,有优异的耐磨性.它们的晶体结构如图所示.
氮化硼(BN)晶体有多种相结构.六方相氮化硼是通常存在的稳定相,与石墨相似,只有层状结构,可作高温润滑剂.立方相氮化硼是超硬材料,有优异的耐磨性.它们的晶体结构如图所示.