题目内容
ClO2在常温下是一种黄绿色有刺激性气味的气体,其熔点为-59℃,沸点为11.0℃,易溶于水.工业上用稍潮湿的KClO3和草酸(H2C2O4)在60℃时反应制得ClO2、K2CO3和CO2.某学生拟用图1所示装置模拟工业制取并收集ClO2.

(1)A装置中发生反应的化学方程式是 .A装置必须添加温度控制装置,除酒精灯外,还需要的玻璃仪器有烧杯、 .
(2)B装置必须放在冰水浴中,其原因是 .
(3)反应后在装置C中可得NaClO2溶液.已知(1)NaClO2饱和溶液在温度低于38℃时析出晶体是NaClO2?3H2O,在温度高于38℃时析出晶体是NaClO2,温度高于60℃时NaClO2分解生成NaClO3和NaCl;(2)NaClO2的溶解度曲线如图2所示,请补充从NaClO2溶液中制得NaClO2晶体的操作步骤:
① ;② ;③洗涤;④低于60℃干燥;得到成品.
(4)ClO2很不稳定,需随用随制,产物用水吸收得到ClO2溶液.为测定所得溶液中ClO2的含量,进行了下列实验:
步骤1:准确量取ClO2溶液10.00mL,稀释成250mL试样;量取V1 mL试样加入到锥形瓶中;
步骤2:用稀硫酸调节试样的pH≤2.0,加入足量的KI晶体,静置片刻;(1molClO2与足量的KI反应转移5mol电子)
步骤3:加入指示剂,用C mol?L-1 Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V2 mL
(已知2Na2S2O3+I2=Na2S4O6+2NaI).
①配制250mL c mol?L-1 Na2S2O3标准溶液时,用到的玻璃仪器除烧杯、量筒、玻璃棒外还有: .
②滴定过程中进行三次平行测定的原因是 .
③若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果 .(填“偏高”、“偏低”或“不变”
④原ClO2溶液的浓度为 g/L(用步骤中的字母代数式表示)

(1)A装置中发生反应的化学方程式是
(2)B装置必须放在冰水浴中,其原因是
(3)反应后在装置C中可得NaClO2溶液.已知(1)NaClO2饱和溶液在温度低于38℃时析出晶体是NaClO2?3H2O,在温度高于38℃时析出晶体是NaClO2,温度高于60℃时NaClO2分解生成NaClO3和NaCl;(2)NaClO2的溶解度曲线如图2所示,请补充从NaClO2溶液中制得NaClO2晶体的操作步骤:
①
(4)ClO2很不稳定,需随用随制,产物用水吸收得到ClO2溶液.为测定所得溶液中ClO2的含量,进行了下列实验:
步骤1:准确量取ClO2溶液10.00mL,稀释成250mL试样;量取V1 mL试样加入到锥形瓶中;
步骤2:用稀硫酸调节试样的pH≤2.0,加入足量的KI晶体,静置片刻;(1molClO2与足量的KI反应转移5mol电子)
步骤3:加入指示剂,用C mol?L-1 Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V2 mL
(已知2Na2S2O3+I2=Na2S4O6+2NaI).
①配制250mL c mol?L-1 Na2S2O3标准溶液时,用到的玻璃仪器除烧杯、量筒、玻璃棒外还有:
②滴定过程中进行三次平行测定的原因是
③若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果
④原ClO2溶液的浓度为
考点:探究物质的组成或测量物质的含量,常见气体制备原理及装置选择
专题:
分析:(1)工业上用稍潮湿的KClO3和草酸(H2C2O4)在60℃时反应制得ClO2、K2CO3和CO2,根据反应物、产物和反应条件写出反应方程式;让反应物充分的接触;测量温度的仪器是温度计;
(2)二氧化氯的熔点较低,为收集二氧化氯,应在较低温度下进行;
(3)从溶液中制取溶质,一般采用蒸发结晶、过滤、洗涤、干燥的方法;
(4)①配制250mL c mol?L-1 Na2S2O3标准溶液时,应选择250mL容量瓶.定容需要胶头滴管;
②多次实验可以减少误差;
③把空气的体积算在内;
④多次实验可以减少误差,根据关系式2ClO2~5I2~10Na2S2O3计算c(ClO2).
(2)二氧化氯的熔点较低,为收集二氧化氯,应在较低温度下进行;
(3)从溶液中制取溶质,一般采用蒸发结晶、过滤、洗涤、干燥的方法;
(4)①配制250mL c mol?L-1 Na2S2O3标准溶液时,应选择250mL容量瓶.定容需要胶头滴管;
②多次实验可以减少误差;
③把空气的体积算在内;
④多次实验可以减少误差,根据关系式2ClO2~5I2~10Na2S2O3计算c(ClO2).
解答:
解:(1)让反应物充分的接触,加快反应速率反应时搅拌,测量温度的仪器是温度计;加热60℃,氯酸钾和草酸反应生成碳酸钾、二氧化碳、二氧化氯和水,反应方程式为:2KClO3+H2C2O4
K2CO3+CO2↑+2ClO2↑+H2O,
故答案为:2KClO3+H2C2O4
K2CO3+CO2↑+2ClO2↑+H2O;温度计;
(2)二氧化氯的熔点较低,为收集二氧化氯,应在较低温度下进行,所以应该采用冰水浴,
故答案为:使ClO2充分冷凝,减少挥发;
(3)从溶液中制取溶质,一般采用蒸发结晶、过滤、洗涤、干燥的方法,为防止析出晶体NaClO2?3H2O,
趁热过滤;用38℃~60℃热水洗涤;低于60℃干燥;
故答案为:蒸发结晶;趁热过滤;
(4))①配制250mL c mol?L-1 Na2S2O3标准溶液时,应选择250mL容量瓶,定容需要胶头滴管;
故答案为:250mL 容量瓶、胶头滴管;
②为减少实验误差,应采用多次实验的方法,故答案为:取平均值,减少计算误差;
③把空气的体积算在内,故读出的消耗的体积就偏大,故测定结果偏高,故答案为:偏高;
④设原ClO2溶液的浓度为x,
2ClO2~5I2~10Na2S2O3
2mol 10mol
mol 1×10-3cV2mol
x=
mol?L-1=
mol/L×67.5g/mol=
g?L-1,
故答案为:
.
| ||
故答案为:2KClO3+H2C2O4
| ||
(2)二氧化氯的熔点较低,为收集二氧化氯,应在较低温度下进行,所以应该采用冰水浴,
故答案为:使ClO2充分冷凝,减少挥发;
(3)从溶液中制取溶质,一般采用蒸发结晶、过滤、洗涤、干燥的方法,为防止析出晶体NaClO2?3H2O,
趁热过滤;用38℃~60℃热水洗涤;低于60℃干燥;
故答案为:蒸发结晶;趁热过滤;
(4))①配制250mL c mol?L-1 Na2S2O3标准溶液时,应选择250mL容量瓶,定容需要胶头滴管;
故答案为:250mL 容量瓶、胶头滴管;
②为减少实验误差,应采用多次实验的方法,故答案为:取平均值,减少计算误差;
③把空气的体积算在内,故读出的消耗的体积就偏大,故测定结果偏高,故答案为:偏高;
④设原ClO2溶液的浓度为x,
2ClO2~5I2~10Na2S2O3
2mol 10mol
| 10-2×x×V1×10-3 |
| 0.25 |
x=
| 5cV2 |
| V1 |
| 5cV2 |
| V1 |
| 337.5CV2 |
| V1 |
故答案为:
| 337.5CV2 |
| V1 |
点评:本题考查实验方案的设计,同时考查学生分析问题、解决问题的能力,明确物质的性质是解本题关键,难度中等.

练习册系列答案
相关题目
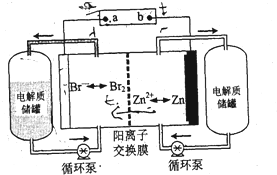 锌溴液流电池是一种新型电化学储能装置(如图所示)电解液为溴化锌水溶液,电解液在电解质储罐和电池间不断循环,下列说法正确的是( )
锌溴液流电池是一种新型电化学储能装置(如图所示)电解液为溴化锌水溶液,电解液在电解质储罐和电池间不断循环,下列说法正确的是( )| A、充电时电极b连接电源的正极 |
| B、放电时正极的电极反应式为Zn-2e-=Zn2+ |
| C、阳离子交换膜可阻止Br2与Zn直接发生反应 |
| D、充电时左侧电解质储罐中的离子总浓度增大 |
在1000mL含等物质的量的HI和H2SO3的溶液里通入0.25molCl2,有二分之一的HI变为I2(已知:I2+H2SO3+H2O=4H++SO42-+2I-).原溶液中HI和H2SO3的浓度都等于( )
| A、0.2mol?L-1 |
| B、0.1mol?L-1 |
| C、2.0mol?L-1 |
| D、1.0mol?L-1 |