题目内容
下列关于稀有气体的叙述不正确的是( )
| A、原子的最外电子数都有8个电子 |
| B、其原子与下一周期IA、IIA族阳离子具有相同的核外电子排布 |
| C、化学性质非常不活泼 |
| D、不能形成双原子分子 |
考点:元素周期表的结构及其应用,元素周期律的作用
专题:元素周期律与元素周期表专题
分析:A.稀有气体均为单原子构成的分子,性质稳定,原子结构与下一周期IA、IIA族阳离子具有相同的核外电子排布,满足8电子稳定结构,只有He为2电子,以此来解答.
解答:
解:A.He的最外电子数为2个电子,其它稀有气体原子的最外电子数都有8个电子,故A错误;
B.稀有气体原子结构与下一周期IA、IIA族阳离子具有相同的核外电子排布,满足8电子稳定结构,或2个电子稳定结构,故B正确;
C.稀有气体的原子结构均满足最外层电子稳定结构,则性质稳定,故C正确;
D.稀有气体的原子结构均满足最外层电子稳定结构,则均为单原子构成的分子,故D正确;
故选A.
B.稀有气体原子结构与下一周期IA、IIA族阳离子具有相同的核外电子排布,满足8电子稳定结构,或2个电子稳定结构,故B正确;
C.稀有气体的原子结构均满足最外层电子稳定结构,则性质稳定,故C正确;
D.稀有气体的原子结构均满足最外层电子稳定结构,则均为单原子构成的分子,故D正确;
故选A.
点评:本题考查元素周期表的结构及应用,为高频考点,把握稀有气体原子结构与性质的关系为解答的关键,注意He为例外,题目难度不大.

练习册系列答案
相关题目
实验室中需要配制2mol/L的NaCl溶液950mL,配制时应称取的NaCl的质量是( )
| A、111.2g |
| B、1112.0g |
| C、117.0g |
| D、1170.0g |
下列关于NO、NO2的说法中,错误的是( )
| A、NO2是红棕色气体 |
| B、NO2有刺激性气味 |
| C、NO是黄绿色气体 |
| D、NO能与血红蛋白结合,有毒 |
在一个密闭容器内有X、Y、Z、Q四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表:
试判断该密闭容器中发生反应属于( )
| 物质 | X | Y | Z | Q |
| 反应前质量/g | 2 | 2 | 48 | 5 |
| 反应后质量/g | 待测 | 24 | 0 | 14 |
| A、化合反应 | B、置换反应 |
| C、复解反应 | D、分解反应 |
用NaOH固体配制1.0mol/L的NaOH溶液220mL,下列说法正确的是( )
| A、首先称取NaOH固体8.8g |
| B、定容时仰视刻度线会使所配制的溶液浓度偏高 |
| C、定容后将溶液振荡均匀,静置时发现液面低于刻度线,于是又加少量水至刻度线 |
| D、容量瓶中原有少量蒸馏水对结果没有影响 |
下列各组物质的熔点变化规律,与它们的化学键无关的是( )
| A、F2、Cl2、Br2、I2的熔点依次升高 |
| B、Li、Na、K、Rb的熔点依次降低 |
| C、NaF、NaCl、NaBr、NaI的熔点依次降低 |
| D、晶体硅、碳化硅、金刚石熔点依次升高 |
经研究发现,有一种磷分子具有链状结构,其结构简式为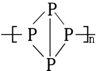 ,下列说法正确的是( )
,下列说法正确的是( )
 ,下列说法正确的是( )
,下列说法正确的是( )| A、它是一种高分子化合物 |
| B、它的分子中具有极性共价键 |
| C、分子中每个磷原子以三个共价健分别结合三个磷原子 |
| D、分子中具有不饱和键 |
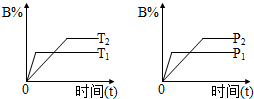 某可逆反应:mA(g)+nB(g)?pC(g);在密闭容器中进行,如图所示,反应在不同时间t、温度T和压强p与反应物B在混合气体中的百分含量(B%)的关系曲线,由曲线分析下列判断正确的是( )
某可逆反应:mA(g)+nB(g)?pC(g);在密闭容器中进行,如图所示,反应在不同时间t、温度T和压强p与反应物B在混合气体中的百分含量(B%)的关系曲线,由曲线分析下列判断正确的是( )| A、T1<T2,p1>p2,n+m>p,(正反应为吸热反应) |
| B、T1>T2,p1>p2,n+m>p,(正反应为吸热反应) |
| C、T1>T2,p1>p2,n+m<p,(正反应为吸热反应) |
| D、T1>T2,p1>p2,n+m>p,(正反应为放热反应) |
下列各组物质的溶液,两者相互滴加现象不同的是( )
| A、FeCl3和NaOH |
| B、NaHCO3和HCl |
| C、NaAlO2和HCl |
| D、AlCl3和NH3?H2O |