题目内容
14.下列叙述不正确的是( )| A. | 原电池是将化学能转化为电能的装置 | |
| B. | 铁船底镶嵌锌块,锌作负极,以防船体被腐蚀 | |
| C. | 钢铁腐蚀的负极反应:Fe-3e-═Fe3+ | |
| D. | 把锌片放入盛有盐酸的试管中,加入几滴氯化铜溶液,气泡放出速率加快 |
分析 A、原电池的实质为氧化还原反应,实现能量转化;
B、原电池放电时,负极被腐蚀,正极被保护;
C、钢铁发生腐蚀时,负极上发生氧化反应,正极上发生还原反应;
D、形成原电池加快反应速率.
解答 解:A、原电池是将化学能转化为电能的装置,故A正确;
B、铁、锌和电解质溶液构成原电池时,较活泼的金属锌作负极,铁作正极,负极上锌失电子被腐蚀,正极铁上得电子发生还原反应被保护,故B正确;
C、钢铁腐蚀时,负极上铁失电子生成二价铁离子,所以电极反应式为Fe-2e-=Fe2+,故C错误;
D、锌粒和氯化铜反应生成Cu,Cu-Zn-盐酸能形成原电池,加快反应速率,故D正确;
故选C.
点评 本题考查了金属的腐蚀与防护,易错选项是C,注意铁发生腐蚀时生成二价铁离子不是三价铁离子.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
4.分类是学习和研究化学的一种常用的科学方法.下列分类合理的是( )
①根据酸分子中含有H原子个数将酸分为一元酸、二元酸等
②根据丁达尔现象可将分散系分为胶体、溶液和浊液
③Al2O3是两性氧化物,能与NaOH溶液反应
④根据反应的热效应将化学反应分为放热反应和吸热反应.
①根据酸分子中含有H原子个数将酸分为一元酸、二元酸等
②根据丁达尔现象可将分散系分为胶体、溶液和浊液
③Al2O3是两性氧化物,能与NaOH溶液反应
④根据反应的热效应将化学反应分为放热反应和吸热反应.
| A. | ①③④ | B. | ③④ | C. | ②③④ | D. | ①②③ |
5.如图所示,某同学设计了一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜.下列有关说法正确的是( )
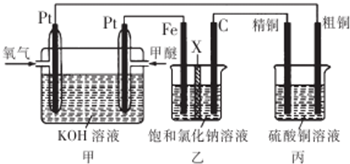

| A. | 通入氧气的一极为正极,发生的电极反应为O2-4e -+2H2O═4OH- | |
| B. | 乙装置中铁电极为阴极,电极反应式为Fe-2e -═Fe2+ | |
| C. | 反应一段时间后,乙装置中生成的氢氧化钠在铁极区 | |
| D. | 反应一段时间后,丙装置中硫酸铜溶液浓度保持不变 |
2.下列关于NH4+、NH3、NH2-三种微粒的说法不正确的是( )
| A. | 三种微粒所含有的电子数相等 | B. | 三种微粒中氮原子的杂化方式相同 | ||
| C. | 三种微粒的空间构型相同 | D. | 键角大小关系:NH4+>NH3>NH2- |
9.某同学学习了化学反应速率后,联想到曾用H2O2制备氧气,于是设计了下面的实验方案并进行实验探究.
【查阅资料】过氧化氢(H2O2),其水溶液俗称双氧水,常温下是一种无色液体,性质比较稳定.在加热的条件下,它能分解生成氧气.研究表明,将新制的5%的H2O2溶液加热到65℃时就有氧气放出,加热到80℃时就有较多氧气产生.
(1)上述实验发生反应的化学方程式为2H2O2$\frac{\underline{\;\;△\;\;}}{\;}$2H2O+O2↑.
(2)实验甲和实验乙的实验目的是探究反应物的不同浓度对反应速率的影响;实验丙、实验丁和实验戊的实验目的是探究在不同酸碱性条件下,催化剂对反应速率的影响.
(3)请根据该同学查阅的资料分析H2O2的性质,解释实验甲和实验乙能否达到实验目的?
(4)实验过程中该同学对实验丙、丁、戊中产生的气体进行收集,并在2分钟内6个时间点对注射器内气体进行读数,记录数据如表.
①对实验戊,0~20s的反应速率v1=0.775mL/s,100~120s的反应速率v2=0.575mL/s.不考虑实验测量误差,二者速率存在差异的主要原因是随反应的不断进行,H2O2溶液的浓度逐渐降低,反应速率减小.
②如图是根据实验收集到最大体积的气体时所用时间绘制的图象.曲线c表示的是实验丁(填“丙”、“丁”或“戊”).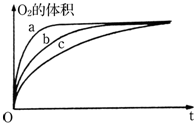
| 实验编号 | 反应物 | 催化剂 |
| 甲 | 试管中加入3mL 2%H2O2溶液和3滴蒸馏水 | 无 |
| 乙 | 试管中加入3mL 5%H2O2溶液和3滴蒸馏水 | 无 |
| 丙 | 试管中加入3mL 5%H2O2溶液和3滴蒸馏水 | 1mL 0.1mol/L FeCl3溶液 |
| 丁 | 试管中加入3mL 5%H2O2溶液和3滴稀盐酸溶液 | 1mL 0.1mol/L FeCl3溶液 |
| 戊 | 试管中加入3mL 5%H2O2溶液和3滴NaOH溶液 | 1mL 0.1mol/L FeCl3溶液 |
(1)上述实验发生反应的化学方程式为2H2O2$\frac{\underline{\;\;△\;\;}}{\;}$2H2O+O2↑.
(2)实验甲和实验乙的实验目的是探究反应物的不同浓度对反应速率的影响;实验丙、实验丁和实验戊的实验目的是探究在不同酸碱性条件下,催化剂对反应速率的影响.
(3)请根据该同学查阅的资料分析H2O2的性质,解释实验甲和实验乙能否达到实验目的?
(4)实验过程中该同学对实验丙、丁、戊中产生的气体进行收集,并在2分钟内6个时间点对注射器内气体进行读数,记录数据如表.
| 时间/s | 20 | 40 | 60 | 80 | 100 | 120 | |
| 气体体积/mL | 实验丙 | 9.5 | 19.5 | 29.0 | 36.5 | 46.0 | 54.5 |
| 实验丁 | 8.0 | 16.0 | 23.5 | 31.5 | 39.0 | 46.5 | |
| 实验戊 | 15.5 | 30.0 | 44.5 | 58.5 | 71.5 | 83.0 | |
②如图是根据实验收集到最大体积的气体时所用时间绘制的图象.曲线c表示的是实验丁(填“丙”、“丁”或“戊”).

19.NA为阿伏加德罗常数的数值,下列说法中正确的是( )
| A. | 一定条件下,2.3g的Na完全与O2反应生成3.6g产物时失去的电子数为0.1NA | |
| B. | 在密闭容器中加入l.5mol H2和0.5molN2,充分反应后得到NH3分子数为NA | |
| C. | 1.0L的0.1 mol•L-1Na2S溶液中含有的S2-离子数为0.1NA | |
| D. | 标准状况下,22.4L的CCl4中含有的CCl4分子数为NA |
6.链型的不饱和油酸(C17H33COOH)与蔗糖反应可以制得非天然油脂,其反应示意图如图所示(图中的反应式不完整),则下列说法不正确的是( )
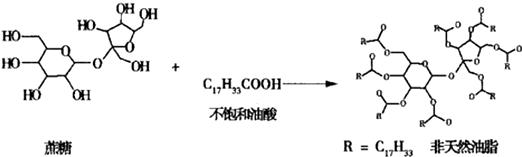

| A. | 该非天然油脂与氢氧化钠溶液共热,产物可与溴的四氯化碳溶液反应 | |
| B. | 天然油脂、蔗糖、非天然油脂都能发生水解反应 | |
| C. | 蔗糖、葡萄糖分别与银氨溶液水浴加热反应,有相同的实验现象 | |
| D. | 植物油、非天然油脂都可以与H2发生加成反应 |
20.一种新型熔融盐燃料电池具有高发电效率,现用Li2CO3和Na2CO3的熔融盐混合物作电解质,一极通CO气体,另一极通O2和CO2混合气体,其总反应为:2CO+O2═2CO2,则下列说法中正确的是( )
| A. | 通CO的一极是电池的负极 | |
| B. | 负极发生的电极反应是:O2+2CO2+4e-═2CO32- | |
| C. | 正极发生的电极反应是:CO+CO32--2e-═2CO2 | |
| D. | 正极发生还原反应 |