题目内容
按照下列元素基态原子的电子排布特征判断元素,并回答问题:
A原子的3p轨道上得到一个电子后不能再容纳外来电子;B原子的2p轨道上有一个电子的自旋方向与2p轨道上其他电子的自旋方向相反;C原子的第三电子层上有8个电子,第四层上只有1个电子;D元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子.
(1)A~D分别是哪种元素(用元素符号填空):
A: ;B: ;C: ;D: ;
(2)写出 DA2的溶液中离子浓度大小关系 .
(3)写出用惰性电极电解电解CA溶液的化学方程式 .
A原子的3p轨道上得到一个电子后不能再容纳外来电子;B原子的2p轨道上有一个电子的自旋方向与2p轨道上其他电子的自旋方向相反;C原子的第三电子层上有8个电子,第四层上只有1个电子;D元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子.
(1)A~D分别是哪种元素(用元素符号填空):
A:
(2)写出 DA2的溶液中离子浓度大小关系
(3)写出用惰性电极电解电解CA溶液的化学方程式
考点:原子结构与元素的性质
专题:原子组成与结构专题,元素周期律与元素周期表专题
分析:A原子3p轨道上得到1个电子后不能再容纳外来电子,则A是Cl元素;B原子的2p轨道上有1个电子的自旋方向与其它电子的自旋方向相反,核外电子排布为1s22s22p4,则B是O元素;C原子的第三电子层上有8个电子,第四层上只有1个电子,则C是K元素;D元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,原子核外电子数=2+8+18+1=29,则D为Cu,据此解答.
解答:
解:A原子3p轨道上得到1个电子后不能再容纳外来电子,则A是Cl元素;B原子的2p轨道上有1个电子的自旋方向与其它电子的自旋方向相反,核外电子排布为1s22s22p4,则B是O元素;C原子的第三电子层上有8个电子,第四层上只有1个电子,则C是K元素;D元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,原子核外电子数=2+8+18+1=29,则D为Cu,
(1)由上述分析可知,A为Cl元素,B为O元素,C为K元素,D为Cu,故答案为:Cl;O;K;Cu;
(2)CuCl2的溶液中Cl-离子浓度最大,Cu2+离子水解,溶液呈酸性,水解程度微弱,铜离子浓度远远大于氢离子浓度,故溶液中离子浓度大小关系为:c(Cl-)>c(Cu2+)>c(H+)>c(OH-),
故答案为:c(Cl-)>c(Cu2+)>c(H+)>c(OH-);
(3)用惰性电极电解电解KCl溶液的化学方程式为2KCl+2H2O
2KOH+H2↑+Cl2↑,
故答案为:2KCl+2H2O
2KOH+H2↑+Cl2↑.
(1)由上述分析可知,A为Cl元素,B为O元素,C为K元素,D为Cu,故答案为:Cl;O;K;Cu;
(2)CuCl2的溶液中Cl-离子浓度最大,Cu2+离子水解,溶液呈酸性,水解程度微弱,铜离子浓度远远大于氢离子浓度,故溶液中离子浓度大小关系为:c(Cl-)>c(Cu2+)>c(H+)>c(OH-),
故答案为:c(Cl-)>c(Cu2+)>c(H+)>c(OH-);
(3)用惰性电极电解电解KCl溶液的化学方程式为2KCl+2H2O
| ||
故答案为:2KCl+2H2O
| ||
点评:本题考查结构与位置关系、核外电子排布、离子浓度比较、电解原理等,比较基础,明确元素种类是解答的关键,注意对基础知识的掌握.

练习册系列答案
 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案 高效智能课时作业系列答案
高效智能课时作业系列答案
相关题目
下列各组物质中,能用分液漏斗进行分离的是( )
| A、四氯化碳和液溴 |
| B、汽油和花生油 |
| C、苯和食盐水 |
| D、酒精和水 |
下列说法正确的是( )
| A、9g水和标准状况下11.2LH2O所含分子数相同 |
| B、同温同压下,氦气的体积是氢气的两倍,则氦原子数与氢原子数之比为2:1 |
| C、同温同压,相同质量的CO和N2具有相同体积 |
| D、不同气体若体积不同,它们所含分子数也不同 |
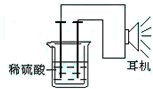 利用生活中或实验室中常用的物品,根据氧化还原反应知识和电学知识,自己动手设计一个原电池.请填写下列空白:
利用生活中或实验室中常用的物品,根据氧化还原反应知识和电学知识,自己动手设计一个原电池.请填写下列空白:
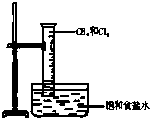 如图所示,将等物质的量的Cl2和CH4 充入一容积为 25mL的量筒,并将量筒倒置在盛有饱和食盐水的水槽中,用日光散射,可观察到的现象是;
如图所示,将等物质的量的Cl2和CH4 充入一容积为 25mL的量筒,并将量筒倒置在盛有饱和食盐水的水槽中,用日光散射,可观察到的现象是;