题目内容
(1)实验前,关闭活塞b,试管d中加水至浸没长导管口,塞紧试管c和d的胶塞,加热c,其目的是
(2)在d中加适量NaOH溶液,c中放一小块铜片,由分液漏斗a向c中加入2mL浓硝酸.c中反应的化学方程式是
(3)上表是制取硝酸铜的三种方案,能体现绿色化学理念的最佳方案是
(4)该小组还用上述装置进行实验证明氧化性KMnO4>Cl2>Br2,则c中加入的试剂是
d中加入的试剂是

(2)根据铜与浓硝酸反应得到硝酸铜、二氧化氮和水;根据二氧化氮能与水反应;
(3)根据制备过程中耗酸量最少,无污染的原则;
(4)根据氧化还原反应中氧化剂的氧化性大于氧化产物的氧化性,利用KMnO4与浓盐酸反应,再利用产生的氯气与KBr溶液反应得到溴,同时要注意尾气吸收;
(2)因铜与浓硝酸反应:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,由a向c中加2mL蒸馏水,硝酸进行的稀释,反应变缓,同时因二氧化氮能与水反应:3NO2+2H2O=2HNO3+NO,c中气体颜色变浅,故答案为:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O;反应变缓,气体颜色变淡;
(3)铜与浓硝酸制取硝酸铜时的方程式是:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,生成的NO2会造成大气污染,硝酸的利用率为
| 1 |
| 2 |
铜与稀硝酸制取硝酸铜时的方程式是:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O,生成的NO也会造成大气污染,硝酸的利用率为
| 3 |
| 4 |
此过程用方程式可表示为:2Cu+O2
| ||
(4)根据氧化还原反应中氧化剂的氧化性大于氧化产物的氧化性,利用KMnO4与浓盐酸反应:2KMnO4KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O,
再利用产生的氯气与KBr溶液反应得到溴:Cl2+2KBr=2KCl+Br2,所以c中有黄绿色气体产生,d中溶液变为黄棕色,同时要注意尾气吸收,
故答案为:KMnO4;KBr溶液(含Br-的溶液);c中有黄绿色气体产生,d中溶液变为黄棕色;没有处理尾气.

 名校课堂系列答案
名校课堂系列答案(12分)某兴趣小组设计出下图所示装置来改进教材中“铜与硝酸反应”实验,以探究化学实验的绿色化。
(1)实验前,关闭活塞b,试管d中加水至浸没长导管口,塞紧试管c和d的胶塞,加热c。其目的是 。
(2)在d中加适量NaOH溶液,c中放一小块铜片,由分液漏斗a向c中加入2 mL浓硝酸。c中反应的化学方程式是 。再由a向c中加2 mL蒸馏水,c中的实验现象是 。
(3)下表是制取硝酸铜的三种方案,能体现绿色化学理念的最佳方案是 。理由是_____________。
| 方案 | 反应物 |
| 甲 | Cu、浓HNO3 |
| 乙 | Cu、稀HNO3 |
| 丙 | Cu、O2、稀HNO3 |
(4)该小组还用上述装置进行实验证明氧化性KMnO4>Cl2>Br2。操作步骤为 ,实验现象 ;但此实验的不足之处是 。
(12分)某兴趣小组设计出下图所示装置来改进教材中“铜与硝酸反应”实验,以探究化学实验的绿色化。
(1)实验前,关闭活塞b,试管d中加水至浸没长导管口,塞紧试管c和d的胶塞,加热c。其目的是 。
(2)在d中加适量NaOH溶液,c中放一小块铜片,由分液漏斗a向c中加入2 mL浓硝酸。c中反应的化学方程式是 。再由a向c中加2 mL蒸馏水,c中的实验现象是 。
(3)下表是制取硝酸铜的三种方案,能体现绿色化学理念的最佳方案是 。理由是_____________。
方案 | 反应物 |
| 甲 | Cu、浓HNO3 |
| 乙 | Cu、稀HNO3 |
| 丙 | Cu、O2、稀HNO3 |
(4)该小组还用上述装置进行实验证明氧化性KMnO4>Cl2>Br2。操作步骤为 ,实验现象 ;但此实验的不足之处是 。
(12分)某兴趣小组设计出下图所示装置来改进教材中“铜与硝酸反应”实验,以探究化学实验的绿色化。
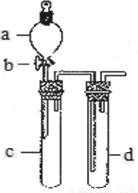
(1)实验前,关闭活塞b,试管d中加水至浸没长导管口,塞紧试管c和d的胶塞,加热c。其目的是 。
(2)在d中加适量NaOH溶液,c中放一小块铜片,由分液漏斗a向c中加入2 mL浓硝酸。c中反应的化学方程式是 。再由a向c中加2 mL蒸馏水,c中的实验现象是 。
(3)下表是制取硝酸铜的三种方案,能体现绿色化学理念的最佳方案是 。理由是_____________。
|
方案 |
反应物 |
|
甲 |
Cu、浓HNO3 |
|
乙 |
Cu、稀HNO3 |
|
丙 |
Cu、O2、稀HNO3 |
(4)该小组还用上述装置进行实验证明氧化性KMnO4>Cl2>Br2。操作步骤为 ,实验现象 ;但此实验的不足之处是 。

