题目内容
17.下表列出了A~R 9种元素在周期表中的位置,请回答下列问题:| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | A | B | ||||||
| 3 | C | D | E | F | H | |||
| 4 | G | R |
(2)E元素的最高价氧化物对应的水化物与氢氧化钠溶液反应的离子方程式是Al(OH)3+OH-=AlO2-+2H2O;
(3)D、E、A三种元素按原子半径由大到小的顺序排列的是Mg>Al>C(用元素符号表示);
(4)B元素最常见的氢化物的化学式是H2O,该氢化物在常温下跟G发生反应的化学方程式是2K+2H2O=2KOH+H2↑,所得溶液的pH>7(填“>”、“<”或“=”);
(5)R元素跟C元素形成的化合物的化学式是NaBr,高温灼烧该化合物时,火焰呈黄色;
(6)F和R元素两者核电荷数之差是18.
分析 (1)由元素在周期表的位置确定元素,稀有气体的性质最不活泼;
(2)E元素的最高价氧化物对应的水化物为氢氧化铝,与氢氧化钠溶液反应生成偏铝酸钠和水;
(3)电子层越多,原子半径越大,同周期从左向右原子半径减小;
(4)B元素最常见的氢化物为水,与K反应生成KOH和氢气;
(5)R元素跟C元素形成的化合物为NaBr,钠的焰色反应为黄色;
(6)F和R元素的核电荷数分别为17、35.
解答 解:(1)由元素在周期表的位置可知,A为C、B为O、C为Na、D为Mg、E为Al,用中文名称表示元素F为 氯,G为钾,H为氩,R为溴,其中化学性质最不活泼的元素为Ar,其质子数是18,
故答案为:C;O;Na;Mg;Al;氯; 钾;氩; 溴;18;
(2)E元素的最高价氧化物对应的水化物为氢氧化铝,与氢氧化钠溶液反应生成偏铝酸钠和水,离子反应为Al(OH)3+OH-=AlO2-+2H2O,
故答案为:Al(OH)3+OH-=AlO2-+2H2O;
(3)电子层越多,原子半径越大,同周期从左向右原子半径减小,则D、E、A三种元素按原子半径由大到小的顺序排列的是Mg>Al>C,
故答案为:Mg>Al>C;
(4)B元素最常见的氢化物的化学式是H2O,该氢化物在常温下跟G发生反应的化学方程式是2K+2H2O=2KOH+H2↑,溶液溶质为KOH,所得溶液的pH>7,
故答案为:H2O;2K+2H2O=2KOH+H2↑;>;
(5)R元素跟C元素形成的化合物的化学式是NaBr,高温灼烧该化合物时,火焰呈黄色,故答案为:NaBr;黄;
(6)F和R元素的核电荷数分别为17、35,二者之差为35-17=18,故答案为:18.
点评 本题考查位置、结构、性质,为高频考点,把握元素的位置、性质、元素化合物知识为解答的关键,侧重分析与应用能力的考查,注意氢氧化铝为两性氧化物,题目难度不大.

 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案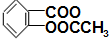 )2]的消炎作用比阿司匹林强十多倍,它为亮蓝色结晶粉末,遇强酸解离为阿司匹林(
)2]的消炎作用比阿司匹林强十多倍,它为亮蓝色结晶粉末,遇强酸解离为阿司匹林(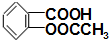 ,M=180)和Cu2+;
,M=180)和Cu2+;已知:
| 阿司匹林溶解质量 | 阿司匹林铜的溶解质量 | |
| 氯仿 | 0.4g | 不溶 |
| 无水乙醇 | 0.9g | 不溶 |
| 蒸馏水 | 不溶 | 不溶 |
阿司匹林$→_{②Naoh溶液}^{①95%乙醇}$阿司匹林钠$→_{15-20℃}^{CuSO_{4}溶液}$ $\stackrel{操作A}{→}$阿司匹林铜
实验二:阿司匹林铜纯度的测定
称取80℃干燥至恒重的阿司匹林铜样品1.0g,置于碘量瓶中,加5mL 6mol•L-1HCl,充分反应后加蒸馏水30mL摇匀,再加入2gKI摇匀,用0.1mol•L-1Na2S2O3溶液滴定至近终点时,加入100g•L-1KSCN试剂1mL,并加入2mL0.5%淀粉溶液,滴定至终点时共消耗Na2S2O3溶液体积为18.60mL.
已知:2Cu2++4I-═2CuI+I2;
I2+2S2O32-═2I-+S4O62-;
CuI+SCN-═CuSCN+I-
回答下列问题:
(1)Na2S2O3溶液应装在碱式滴定管中(填“酸式”或“碱式”);
(2)操作A包括三个实验操作,依次为过滤、洗涤、干燥;
(3)在实验一中采用不同原料比进行实验,得到下表的数据;
| 实验编号 | 阿司匹林:无水硫酸铜/物质的量之比 | 产率% | ||
| X1 | X2 | 平均值 | ||
| 1 | 1:1 | 76.6 | 78.1 | 77.4 |
| 2 | 2:1 | 78.6 | 75.1 | 76.8 |
| 3 | 3:1 | 93.9 | 95.9 | 94.9 |
(4)下列试剂中,洗涤阿司匹林铜最适宜的为B(填字母);
A.碳酸氢钠溶液 B.氯化铁溶液 C.红色石蕊试液 D.新制氢氧化铜悬浊液
(5)实验二中判断到达滴定终点的现象是滴入最后一滴Na2S2O3溶液,蓝色褪去,且半分钟内不恢复蓝色;
(6)碘化亚铜会强力吸附碘单质,实验中如果不加入KSCN试剂会使实验结果偏低(填“偏高”、“偏低”或“无影响”);
(7)阿司匹林铜样品的纯度为78.5%(保留小数点后面1位)
(2)现有一杯具有永久硬度的水,其中主要含有MgCl2、CaCl2.利用下列试剂中的一部分或全部,设计软化该水的实验方案.可选试剂:①Ca(OH)2溶液;②NaOH溶液;③饱和Na2CO3溶液;④肥皂水.实验方案:(填写下表)
| 实验步骤 |
| 向硬水中加入①(填序数),直到不再产生沉淀为止. |
| 继续向溶液中加入③(填序数),直到不再产生沉淀为止. |
| 将上述混合物过滤(填操作) |
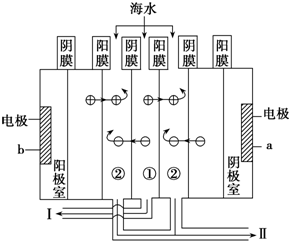
a接电源的负极,Ⅰ口排出的是淡水(填“淡水”或“海水”);
(4)在(3)中某口排出的浓海水中溴元素的质量分数为a%,现用氯气将其中的溴离子氧化为溴单质,则处理1 000t该浓海水需标准状况下的氯气的体积为1400am3.
| A. | 2Na2O2+2H2O═4NaOH+O2↑ | B. | NH3+HCl═NH4Cl | ||
| C. | 2 NaOH+SO2═Na2SO3+H2O | D. | AlCl3+3NH3•H2O═Al(OH)3↓+3NH4Cl |
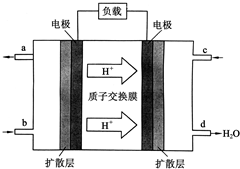 中国科学院长春应用化学研究所在甲烷燃料电池技术方面获得新突破,组装出了自呼吸电池及主动式电堆.甲烷燃料电池的工作原理如图所示.
中国科学院长春应用化学研究所在甲烷燃料电池技术方面获得新突破,组装出了自呼吸电池及主动式电堆.甲烷燃料电池的工作原理如图所示. 实验室欲用NaOH固体配制1.0mol•L-1的NaOH溶液240mL:
实验室欲用NaOH固体配制1.0mol•L-1的NaOH溶液240mL: 某校研究性学习小组用已部分生锈(Fe2O3)的废铁屑,制作印刷电路板的腐蚀剂,即FeCl3溶液.实验操作过程如下:
某校研究性学习小组用已部分生锈(Fe2O3)的废铁屑,制作印刷电路板的腐蚀剂,即FeCl3溶液.实验操作过程如下: