题目内容
下列说法中错误的是( )
| A、氨气极易溶于水,可做喷泉实验 |
| B、硅是制造太阳能电池的常用材料 |
| C、NO2与水反应,它既是氧化剂又是还原剂 |
| D、用铁与稀硝酸反应来制备氢气 |
考点:氨的物理性质,氮的氧化物的性质及其对环境的影响,硅和二氧化硅,铁的化学性质
专题:元素及其化合物
分析:A、常温下,1体积水溶解700体积氨气;
B、硅是将太阳能转化为电能的常用材料;
C、从二氧化氮中N的化合价的升降分析;
D、稀硝酸具有强氧化性.
B、硅是将太阳能转化为电能的常用材料;
C、从二氧化氮中N的化合价的升降分析;
D、稀硝酸具有强氧化性.
解答:
解:A、常温下,1体积水溶解700体积氨气,可做喷泉实验,故A正确;
B、硅是将太阳能转化为电能的常用材料,故B正确;
C、NO2与水反应生成硝酸、NO,NO2中N的化合价既有降低又有升高,因此NO2既作氧化剂又作还原剂,故C正确;
D、稀硝酸具有强氧化性,Fe+4HNO3﹙稀﹚=Fe﹙NO3﹚3﹢NO↑﹢2H2O,故D错误;
故选D.
B、硅是将太阳能转化为电能的常用材料,故B正确;
C、NO2与水反应生成硝酸、NO,NO2中N的化合价既有降低又有升高,因此NO2既作氧化剂又作还原剂,故C正确;
D、稀硝酸具有强氧化性,Fe+4HNO3﹙稀﹚=Fe﹙NO3﹚3﹢NO↑﹢2H2O,故D错误;
故选D.
点评:本题考查了元素及其化合物的性质,题目难度一般,注意强氧化性酸和非强氧化性酸在与金属反应时的区别.

练习册系列答案
相关题目
下列事实中,不能用勒夏特列原理解释的是( )
| A、开启啤酒瓶后,瓶中马上泛起大量泡沫 |
| B、在配制硫酸亚铁溶液时加入过量铁粉 |
| C、生产硝酸的过程,氨的催化氧化反应中通过量空气 |
| D、实验室常用排饱和食盐水的方法收集氯气 |
每年由于腐蚀造成的钢铁损失约占年产量的10~20%,金属的防腐十分重要.钢铁防腐方法有许多种,图-1与图-2是两个典型的例子.对其中原理的描述正确的是( )
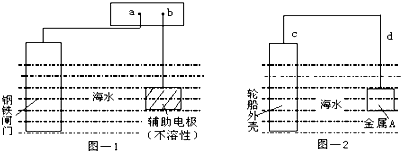

| A、图-1:a为电源正极 |
| B、图-1:辅助电极上发生氧化反应 |
| C、图-2:电流方向d→c |
| D、图-2:金属A可以是耐腐蚀的金属铜 |
对于反应2A(g)+3B(g)=C(g)+5D(g),在某段时间内的平均反应速率为vx,(x代表某反应物或生成物)之间的关系,正确的是( )
A、vA=
| ||
| B、vB=3vC | ||
C、vB=
| ||
D、vB=
|
下列反应中前者属于取代反应,后者属于加成反应的是( )
| A、光照甲烷与氯气的混和物,乙烯使酸性高锰酸钾溶液褪色 | |||
B、CH3CH2-OH+H-O-C2H5
| |||
| C、乙烯使溴的四氯化碳溶液褪色,苯与氢气在一定条件下反应生成环己烷 | |||
| D、在苯中滴入溴水,溴水褪色,乙烯使溴水褪色 |
Na2CO3溶液和NaHCO3溶液共同遵守的关系式是( )
| A、c(Na+)+c(H+)=2c(CO32-)+c(HCO3-)+c(OH-) |
| B、c(Na+)=2[c(CO32-)+c(HCO3-)+c(H2CO3)] |
| C、c(OH-)=c(H+)+c(H2CO3)-c(CO32-) |
| D、c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)>c(H+) |
以Mg片和Al片为电极,并用导线连接,同时插入NaOH溶液中,下列说法正确的是( )
| A、Mg片作负极,电极反应:Mg-2e-=Mg2+ |
| B、电子从Mg电极沿导线流向Al电极 |
| C、Al片作负极,电极反应:Al+4OH--3e-=AlO2-+2H2O |
| D、Al片上有气泡产生 |
下列反应的离子方程式书写正确的是( )
A、用惰性电极电解MgCl2溶液2Cl-+2H2O
| ||||
| B、向Ca(OH)2溶液中加入过量的NaHCO3溶液:Ca2++2HCO3-+2OH-═CO32-+CaCO3↓+2H2O | ||||
| C、次氯酸钙溶液中通入过量的CO2:Ca2++3ClO-+H2O+CO2═CaCO3↓+2HClO | ||||
| D、氢氧化铁溶于碘化氢溶液:Fe(OH)3+3H+═Fe3++3H2O |