题目内容
4.某固体由一种元素组成,密度:5g/cm3.在棱长为10负7次方cm立方体含20个原子,此元素相对原子质量为?分析 固体体积为10-21cm3,含20个原子,每个原子的质量为$\frac{M}{{N}_{A}}$,根据ρ=$\frac{m}{V}$=$\frac{20M}{{N}_{A}V}$计算.
解答 解:固体体积为10-21cm3,设元素的相对原子质量为M,则NA个原子的质量为Mg,每个原子的质量为$\frac{M}{{N}_{A}}$,含20个原子,则固体质量为20×$\frac{M}{{N}_{A}}$g,
ρ=$\frac{m}{V}$=$\frac{20M}{{N}_{A}V}$,可得$\frac{20M}{6.02×1{0}^{23}×1{0}^{-21}}$=5,M=30,
答:元素相对原子质量为30.
点评 本题考查物质的量的计算,为高频考点,侧重于学生的分析、计算能力的考查,注意把握相关计算公式的运用,难度不大.

练习册系列答案
相关题目
15.常温下,下列各组离子在指定环境下能大量共存的是( )
| A. | 碱性溶液中Na+、Cu2+、HCO${\;}_{3}^{-}$、NO${\;}_{3}^{-}$ | |
| B. | 中性溶液中Na+、Fe3+、OH-、SO${\;}_{4}^{2-}$ | |
| C. | 碱性溶液中Na+、K+、SO${\;}_{4}^{2-}$、CO${\;}_{3}^{2-}$ | |
| D. | 酸性溶液中Na+、K+、NO${\;}_{3}^{-}$、CO${\;}_{3}^{2-}$ |
12.对下列未知盐的稀溶液所含离子的检验中,作出的判断一定正确的是( )
| A. | 加入硝酸银溶液,有白色沉淀生成,可判定含有Cl- | |
| B. | 先加入足量稀盐酸,无沉淀生成,再加BaCl2溶液,产生白色沉淀,可判定含有SO42- | |
| C. | 加入NaOH溶液,有白色沉淀产生,可判定含有Mg2+ | |
| D. | 加入盐酸后有无色、无味气体逸出,此气体能使澄清石灰水变浑浊,可判定含有CO32- |
19.已知有转化关系: $\stackrel{③}{→}$C2H5Br,则反应①、②、③的反应类型分别为( )
$\stackrel{③}{→}$C2H5Br,则反应①、②、③的反应类型分别为( )
 $\stackrel{③}{→}$C2H5Br,则反应①、②、③的反应类型分别为( )
$\stackrel{③}{→}$C2H5Br,则反应①、②、③的反应类型分别为( )| A. | 取代反应、加成反应、取代反应 | B. | 取代反应、取代反应、加成反应 | ||
| C. | 氧化反应、加成反应、加成反应 | D. | 氧化反应、加成反应、取代反应 |
9.按官能团的不同可对有机物进行分类,请指出下列有机物的种类错误的一项( )
| A. | CH 3CH 2CH2 CHO醛类 | B. | 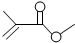 饱和酯类 饱和酯类 | ||
| C. | 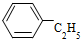 芳香烃 芳香烃 | D. | CH 3CH 2 COOH 羧酸类 |
16.下列物质中,既能与盐酸反应,又能与氢氧化钠溶液反应的是( )
①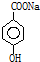 ②NaHCO3 ③Al ④
②NaHCO3 ③Al ④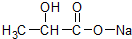 ⑤Al2(SO4)3.
⑤Al2(SO4)3.
①
 ②NaHCO3 ③Al ④
②NaHCO3 ③Al ④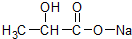 ⑤Al2(SO4)3.
⑤Al2(SO4)3.| A. | ①③ | B. | ③⑤ | C. | ①②③ | D. | ①③④ |
13.NA代表阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 60g丙醇中存在的共价键总数为10NA | |
| B. | 1L 0.1mol•L-1的NaHCO3溶液中HCO3-和CO32-离子数之和为0.1NA | |
| C. | 标准状况下,5.6LCO2与足量Na2O2反应转移的电子数为0.5NA | |
| D. | 2.0gH218O与D2O的混合物中所含中子数为NA |
14.下列混合物分离方法、原理都正确的是( )
| 分离方法 | 原理 | |
| A | 除去乙烯中乙炔:通入酸性高锰酸钾溶液中洗气 | 乙炔能与酸性高锰酸钾溶液反应,而乙烯不反应 |
| B | 分离硝基苯和苯:蒸馏 | 硝基苯和苯的沸点不同 |
| C | 除去丁酸乙酯中乙醇:加入饱和碳酸钠溶液,蒸馏 | 乙醇和丁酸乙酯的沸点不同 |
| D | 用丙醇和氯仿萃取碘水中碘 | 碘易溶于丙醇、氯仿 |
| A. | A | B. | B | C. | C | D. | D |