题目内容
如图是一个化学过程的示意图.已知甲池的总反应式为:2CH3OH+3O2+4KOH
2K2CO3+6H2O
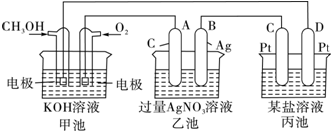
(1)甲电池是 装置,A(石墨)电极的名称是 .
(2)写出电极反应式:通入CH3OH的电极的电极反应式是 .B(Ag)电极的电极反应式为 .
(3)乙池中反应的总反应方程式为 .
(4)当乙池中A(Ag)极的质量增加5.40g时,甲池中理论上消耗O2 mL(标准状况下).
| 放电 |
| 充电 |

(1)甲电池是
(2)写出电极反应式:通入CH3OH的电极的电极反应式是
(3)乙池中反应的总反应方程式为
(4)当乙池中A(Ag)极的质量增加5.40g时,甲池中理论上消耗O2
考点:原电池和电解池的工作原理
专题:电化学专题
分析:(1)甲装置为燃料电池,A与原电池的正极相连;
(2)燃料电池中燃料失电子发生氧化反应,甲醇失电子和氢氧根离子反应生成碳酸根离子和水;B电极与原电池负极相连,为阴极,银离子在B上得电子;
(2)乙为电解池,电解质溶液为AgNO3;
(3)根据电极方程式计算.
(2)燃料电池中燃料失电子发生氧化反应,甲醇失电子和氢氧根离子反应生成碳酸根离子和水;B电极与原电池负极相连,为阴极,银离子在B上得电子;
(2)乙为电解池,电解质溶液为AgNO3;
(3)根据电极方程式计算.
解答:
解:(1)甲装置为甲醇燃料电池,属于原电池,A与原电池的正极相连,则A为阳极;
故答案为:原电池;阳极;
(2)燃料电池中燃料失电子发生氧化反应,甲醇失电子和氢氧根离子反应生成碳酸根离子和水,其电极的电极反应式是CH3OH-6e-+8OH-═6H2O+CO32-;B电极与原电池负极相连,为阴极,银离子在B上得电子,其电极方程式为:Ag++e-=Ag;
故答案为:CH3OH-6e-+8OH-═6H2O+CO32-;Ag++e-=Ag;
(2)乙为电解池,电解质溶液为AgNO3,则乙池中反应的化学方程式为4AgNO3+2H2O
4Ag+O2↑+4HNO3,
故答案为:4AgNO3+2H2O
4Ag+O2↑+4HNO3;
(3)乙池中A(Ag)极上银离子得电子生成Ag,其电极反应为Ag++e-=Ag,已知A(Ag)极的质量增加5.40g时,n(Ag)=
=0.05mol,
则转移电子为0.05mol,甲中正极反应为:O2+4e-+H2O=4OH-,则转移0.05mol电子时消耗的氧气为0.05mol×
=0.0125mol,则氧气的体积为0.0125mol×22.4L/mol=0.28L=280ml
故答案为:280.
故答案为:原电池;阳极;
(2)燃料电池中燃料失电子发生氧化反应,甲醇失电子和氢氧根离子反应生成碳酸根离子和水,其电极的电极反应式是CH3OH-6e-+8OH-═6H2O+CO32-;B电极与原电池负极相连,为阴极,银离子在B上得电子,其电极方程式为:Ag++e-=Ag;
故答案为:CH3OH-6e-+8OH-═6H2O+CO32-;Ag++e-=Ag;
(2)乙为电解池,电解质溶液为AgNO3,则乙池中反应的化学方程式为4AgNO3+2H2O
| ||
故答案为:4AgNO3+2H2O
| ||
(3)乙池中A(Ag)极上银离子得电子生成Ag,其电极反应为Ag++e-=Ag,已知A(Ag)极的质量增加5.40g时,n(Ag)=
| 5.40g |
| 108g/L |
则转移电子为0.05mol,甲中正极反应为:O2+4e-+H2O=4OH-,则转移0.05mol电子时消耗的氧气为0.05mol×
| 1 |
| 4 |
故答案为:280.
点评:本题考查了原电池和电解池原理,明确离子放电顺序是解本题关键,难点是电极反应式的书写,题目难度中等.

练习册系列答案
 一线名师权威作业本系列答案
一线名师权威作业本系列答案
相关题目
若胃酸酸度增高就会患胃酸过多症,下列物不宜用做治疗胃酸过多的药物是 ( )
| A、小苏打粉 | B、氢氧化铝粉 |
| C、氢氧化钠粉 | D、纯碳酸钙粉 |
下列在水溶液中能大量共存的一组是( )
| A、NH4+、Na+、Br-、SO42- |
| B、Fe2+、Al3+、ClO-、Cl- |
| C、Al3+、[A1(OH)4]-、Na+、Cl- |
| D、Mg2+、H+、SiO32-、SO42- |
光照对下列反应几乎无影响的是( )
| A、氢气与氯气 |
| B、甲烷与氯气 |
| C、甲烷与氧气 |
| D、次氯酸分解 |
已知农药波尔多液不能用铁制容器盛放,是因为铁能与农药中的硫酸铜起反应,则下列反应原理和上述原理相同的是( )
| A、氢氧化钠溶液不能用带玻璃塞子的试剂瓶保存 |
| B、澄清石灰水在空气中变质 |
| C、实验室用锌和稀硫酸制氢气 |
| D、氯化钠在水溶液中电离 |
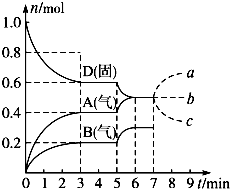 在容积为2.0L的密闭容器内,物质D在T℃时发生反应,其反应物和生成物的物质的量随时间t的变化关系如图,据图回答下列问题:
在容积为2.0L的密闭容器内,物质D在T℃时发生反应,其反应物和生成物的物质的量随时间t的变化关系如图,据图回答下列问题: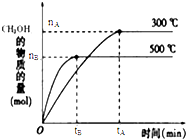 一定条件下,在体积为3L的密闭容器中反应CO(g)+2H2(g)?CH3OH(g)达到化学平衡状态.
一定条件下,在体积为3L的密闭容器中反应CO(g)+2H2(g)?CH3OH(g)达到化学平衡状态.