题目内容
19.室温时,向含有AgCl和AgBr固体的悬浊液中加入少量NaBr固体,下列各项中增大的是( )| A. | c(Ag+) | B. | $\frac{c(C{l}^{-})}{c(B{r}^{-})}$ | C. | c(Cl-) | D. | $\frac{c(A{g}^{+})•c(B{r}^{-})}{c(C{l}^{-})}$ |
分析 室温时,向含有AgCl和AgBr固体的悬浊液中加入少量NaBr固体,NaBr固体是强电解质,溶于水完全电离,所以溶液中的c(Br-)增大,根据室温时AgBr溶度积不变,则c(Ag+)减小,再根据室温时AgCl溶度积不变,则c(Cl-)增大,据此分析.
解答 解:室温时,向含有AgCl和AgBr固体的悬浊液中加入少量NaBr固体,NaBr固体是强电解质,溶于水完全电离,所以溶液中的c(Br-)增大,根据室温时AgBr溶度积不变,则c(Ag+)减小,再根据室温时AgCl溶度积不变,则c(Cl-)增大,又$\frac{c(Ag{\;}^{+})c(C{l}^{-})}{c(Ag{\;}^{+})c(Br{\;}^{-})}$不变,所以$\frac{c(Cl{\;}^{-})}{c(Br{\;}^{-})}$不变,$\frac{c(Ag{\;}^{+})c(Br{\;}^{-})}{c(Cl{\;}^{-})}$减小,故选:C.
点评 本题考查难溶电解质的溶解平衡及沉淀积的应用,注意溶度积只与温度有关,难度不大.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案
相关题目
16.阻燃剂氢氧化铝受热分解时吸收热量,同时生成耐高温的氧化铝和水蒸气,起到防火作用.下列关于该阻燃剂防火原因的分析中错误的是( )
| A. | 氢氧化铝受热分解时吸收燃烧物表面的热量 | |
| B. | 氢氧化铝分解生成的水蒸气稀释燃烧物表面的氧气 | |
| C. | 氢氧化铝受热分解吸收热量使可燃物的着火点降低 | |
| D. | 氢氧化铝分解生成的氧化铝覆盖在燃烧物表面,使燃烧物与O2隔绝 |
17.NA为阿伏加德罗常数,下列说法正确的是( )
| A. | 1molC2H6中含有6 NA个共价键 | |
| B. | 7.8 g Na2O2中含有的阳离子数和阴离子数均为0.2NA | |
| C. | 14.0g由C2H4和C3H6组成的混合气体原子总数为3NA | |
| D. | 5.6g金属铁与足量盐酸反应时失去的电子数是0.3NA |
14. 利用所学知识回答下列问题
利用所学知识回答下列问题
Ⅰ.(1)已知室温下,Ksp[Mg(OH)2]=5×10-12,若溶液中c(Mg2+)=5×10-4 mol/L,则溶液的pH=10.
(2)向1mL0.1mol/LMgCl2溶液中滴加2滴2mol/LNaOH溶液,有白色沉淀生成,再滴加2滴0.1mol/LFeCl3溶液,结果有红褐色沉淀出现.请写出红褐色沉淀生成时的离子方程式3Mg(OH)2+2Fe3+=3Mg2++2Fe(OH)3.
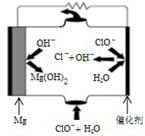
(3)“镁-次氯酸盐”燃料电池的工作原理如图所示,根据图写出镁电极的电极反应式Mg-2e-+2OH-=Mg(OH)2.
Ⅱ.室温下,两种酸的电离平衡常数如下表.
(4)室温下,0.1mol/L Na2CO3溶液的pH>0.1mol/LNa2SO3溶液的pH(选填“>”、“<”或“=”).
(5)0.10mol/L Na2SO3溶液中离子浓度由大到小的顺序为c(Na+)>c(SO32-)>c(OH-)>c(HSO3-)>c(H+).
 利用所学知识回答下列问题
利用所学知识回答下列问题Ⅰ.(1)已知室温下,Ksp[Mg(OH)2]=5×10-12,若溶液中c(Mg2+)=5×10-4 mol/L,则溶液的pH=10.
(2)向1mL0.1mol/LMgCl2溶液中滴加2滴2mol/LNaOH溶液,有白色沉淀生成,再滴加2滴0.1mol/LFeCl3溶液,结果有红褐色沉淀出现.请写出红褐色沉淀生成时的离子方程式3Mg(OH)2+2Fe3+=3Mg2++2Fe(OH)3.
(3)“镁-次氯酸盐”燃料电池的工作原理如图所示,根据图写出镁电极的电极反应式Mg-2e-+2OH-=Mg(OH)2.
Ⅱ.室温下,两种酸的电离平衡常数如下表.
| K1 | K2 | |
| H2SO3 | 1.3×10-2 | 1.0×10-7 |
| H2CO3 | 4.2×10-7 | 5.6×10-11 |
(5)0.10mol/L Na2SO3溶液中离子浓度由大到小的顺序为c(Na+)>c(SO32-)>c(OH-)>c(HSO3-)>c(H+).
4.下列叙述正确的是( )
| A. | 锅炉水垢中的CaSO4经饱和碳酸钠溶液浸泡可转化为CaCO3 | |
| B. | 常温下,在含有Ag+和Cl-的溶液中,Ag+和Cl-浓度之积是个常数 | |
| C. | 当醋酸达到电离平衡后,改变某条件电离平衡向正反应方向移动,则溶液的导电能力一定变强 | |
| D. | 将浓度为0.1 mol/L的HF溶液加水不断稀释,溶液$\frac{c({F}^{-})}{c({H}^{+})}$始终保持增大 |
11.25℃时,已知Ksp(Ag2SO4)=1.2×10-5,Ksp(AgCl)=1.8×10-10,Ksp(Ag2C2O4)=3.5×10-11,Ksp(AgI)=1.5×10-16,该温度下有关叙述正确的是( )
| A. | AgCl、Ag2C2O4、AgI三者的饱和溶液中c(Ag+)大小顺序:Ag2C2O4>AgCl>AgI | |
| B. | 将0.02 mol•L-1AgNO3溶液和0.02 mol•L-1 Na2SO4溶液等体积混合,有沉淀生成 | |
| C. | 向5mL饱和AgCl溶液中滴加0.5mL 0.1 mol•L-1KI溶液,无沉淀生成 | |
| D. | 向浓度均为0.1mol•L-1NaCl和KI混合溶液中滴加AgNO3溶液,先有白色沉淀生成 |
8.化工生产中常用FeS作为沉淀剂除去工业废水中的Pb2+,反应原理为FeS(s)+Pb2+(aq)?PbS(s)+Fe2+(aq),下列有关叙述错误的是( )
| A. | 达到平衡时,c(Pb2+)=c(Fe2+) | |
| B. | Ksp(FeS)大于Ksp(PbS) | |
| C. | 该反应的平衡常数K=$\frac{{K}_{sp}(FeS)}{{K}_{sp}(PbS)}$ | |
| D. | 溶液中加入少量Na2S固体后,c(Fe2+)减小 |
9.下列说法正确的是( )
| A. | 溶度积就是溶解平衡时难溶电解质在溶液中的各离子浓度的乘积 | |
| B. | 溶度积常数是不受任何条件影响的常数,简称溶度积 | |
| C. | 可用离子积Qc与溶度积Ksp的比较来判断沉淀溶解平衡进行的方向 | |
| D. | 所有物质的溶度积都是随温度的升高而增大的 |