题目内容
现有200mLMgCl2、AlCl3的混合溶液,其中c(Mg2+)=0.2mol/L,c(Cl-)=1.3mol/L,要使Mg2+转化为Mg(OH)2并使Mg2+、Al3+mL分离开来,至少需4mol/L的NaOH溶液多少mL?
先根据题中条件,求其中Al3+的浓度:
c(Mg2+)=0.2mol/L,所以与Mg2+结合的Cl-的浓度为0.4mol/L,所以与Al3+结合的Cl-则为1.3-0.4=0.9(mol/L)
所以c(Al3+)=![]()
![]() 0.9=0.3(mpl/L)
0.9=0.3(mpl/L)
在上述混合溶液中,加入NaOH溶液后,Mg2+、Al3+将分别转化为Mg(OH)2沉淀和AlO2-离子,现分别讨论如下:

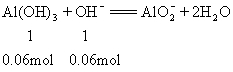
因此,至少需要NaOH溶液的体积为:(0.04![]() 2+0.06
2+0.06![]() 3+0.06)
3+0.06)![]()
![]() =0.08L=80mL
=0.08L=80mL

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目