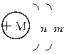题目内容
(1)指出各符号的意义。
(2)确定M、n、l的取值范围。
(3)比较M与(n+l)的大小,得出什么结论?
解答:本题考查了核电荷数与电子数的关系。
(1)+M表示核内有M个质子。n和l分别表示第一层、第二层上分别有n、l个电子。
(2)由核外电子排布规律知,n=2,由于该图可表示原子和离子(阳离子和阴离子),因此,l的取值需分三种情况讨论:
①若表示原子,则l=1,2,3,…,8,故M的取值(M=n+l)为:M=3,4,5,…,10;②若表示阳离子,n=2,l=8,原来第三层上的电子数可能为1,2,3,则l=11,12,13;③若表示阴离子,n=2, l=8,原来第二层上的电子数可能为5、6、7,则M=7, 8, 9。
(3)由核外电子总数与核电荷数的关系知:①当M=n+l时,表示中性原子;②当M>n+l时,表示阳离子,所带电荷数由M-(n+l)确定;③当M<n+l时,表示阴离子,所带电荷数由(n+l)-M确定。

练习册系列答案
相关题目