题目内容
6.保持温度和反应器的体积不变,反应A(g)+3B(g)?2C(g)+4D(s),达平衡后,向该反应器中通入一定量氖气,体系的压强明显增大,如图图象中正确的是( )| A. |  | B. | 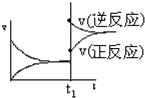 | C. | 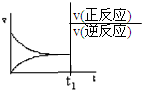 | D. | 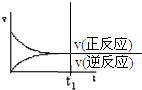 |
分析 温度和容器体积不变,该反应达到平衡状态后,向该反应器中通入一定量氖气,体系的压强明显增大,但参加反应的气体物质的量浓度不变、其分压不变,据此分析解答.
解答 解:温度和容器体积不变,该反应达到平衡状态后,向该反应器中通入一定量氖气,体系的压强明显增大,但参加反应的气体物质的量浓度不变、其分压不变,所以正逆反应速率仍然相等且和原来平衡点相等,所以平衡不移动,故选D.
点评 本题考查压强对化学平衡移动影响原理,为高频考点,改变压强时只有能引起反应物或生成物浓度改变的平衡才发生移动,为易错题.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
16.下列化学用语正确的是( )
| A. | 14C原子的结构示意图: | |
| B. | H2O2的电子式: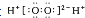 | |
| C. | NH4C的电子式: | |
| D. | 原子核内有10个中子的氧原子${\;}_{8}^{16}$O |
17.普通铜-锌原电池的结构如图,下列有关铜-锌原电池的描述正确的是( )
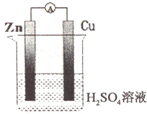

| A. | .锌作负极 | B. | 铜电极上发生氧化反应 | ||
| C. | .铜作负极 | D. | 锌电极上发生还原反应 |
14.某同学采用硫铁矿焙烧取硫后的烧渣 制取七水合硫酸亚铁,设计了如图流程:
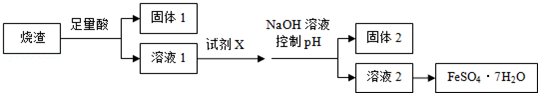
下列说法不正确的是( )

下列说法不正确的是( )
| A. | 溶解烧渣选用足量硫酸,试剂X选用铁粉 | |
| B. | 固体1中一定含有SiO2,控制pH是为了使Al3+转化为Al3,进入固体2 | |
| C. | 从溶液2得到FeSO4•7H2O产品的过程中,须控制条件防止其氧化和分解 | |
| D. | 若改变方案,在溶液1中直接加NaOH至过量,得到的沉淀用硫酸溶解,其溶液经结晶分离也可得到FeSO4•7H2O |
18.某蓄电池放电、充电的反应式为:Fe+Ni2O3+3H2O$?_{放电}^{充电}$Fe(OH)2+2Ni(OH)2,下列推断中正确的是( )
①放电时,Fe为正极,Ni2O3为负极;
②充电时,阴极上的电极反应式是:Fe(OH)2+2e-═Fe+2OH-;
③充电时,Ni(OH)2为阳极;④蓄电池的电极必须浸在某碱性溶液中.
①放电时,Fe为正极,Ni2O3为负极;
②充电时,阴极上的电极反应式是:Fe(OH)2+2e-═Fe+2OH-;
③充电时,Ni(OH)2为阳极;④蓄电池的电极必须浸在某碱性溶液中.
| A. | ①②③ | B. | ①②④ | C. | ①③④ | D. | ②③④ |
15.下列化合物在加热时不能与新制Cu(OH)2反应的是( )
| A. | CH3CHO | B. | CH3CH2OH | C. | HCOOH |
16.设NA代表阿伏伽德罗常数的值,下列叙述正确的是( )
| A. | 标准状况下,18gH218O所含质子数为10NA | |
| B. | 1mol的-OH与1mol的OH-所含电子数均为10NA | |
| C. | 常温常压下,42g乙烯和丁烯混合气体中,极性键数为6NA | |
| D. | Na2O2的反应中,每生成0.1molO2,转移电子数目为0.4NA |
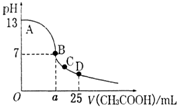 室温下,在25mL 0.1mol.L-1NaOH溶液中逐滴加入0.2mol•L-1 CH3COOH 溶液,pH 与滴加 CH3COOH溶液体积的关系曲线如图所示,若忽略两溶液混合时的体积变化,下列有关粒子浓度关系的说法错误的是( )
室温下,在25mL 0.1mol.L-1NaOH溶液中逐滴加入0.2mol•L-1 CH3COOH 溶液,pH 与滴加 CH3COOH溶液体积的关系曲线如图所示,若忽略两溶液混合时的体积变化,下列有关粒子浓度关系的说法错误的是( )