题目内容
10.下列关于热化学方程式$\frac{1}{2}$H2(g)+$\frac{1}{2}$I2(g)═HI(g)△H=-4.5kJ•mol-1的叙述正确的是( )| A. | 1molH2和1mol I2完全反应放出4.5kJ热量 | |
| B. | 1个氢分子和1个碘分子完全反应放出9kJ热量 | |
| C. | 1molH2和1mol I2完全反应生成气态HI放出9kJ热量 | |
| D. | 0.5mol H2和0.5mol I2完全反应需要吸收4.5kJ热量 |
分析 热化学方程式$\frac{1}{2}$H2(g)+$\frac{1}{2}$I2(g)═HI(g)△H=-4.5kJ•mol-1的意义是$\frac{1}{2}$molH2和$\frac{1}{2}$mol I2完全反应生成气态HI放出4.5kJ热量,化学计量数只代表物质的量,物质的量与能量呈正比.
解答 解:A.热化学方程式$\frac{1}{2}$H2(g)+$\frac{1}{2}$I2(g)═HI(g)△H=-4.5kJ•mol-1的意义是$\frac{1}{2}$molH2和$\frac{1}{2}$mol I2完全反应生成气态HI放出4.5kJ热量,故A错误;
B.化学计量数只代表物质的量,不表示分子个数,故B错误;
C.热化学方程式$\frac{1}{2}$H2(g)+$\frac{1}{2}$I2(g)═HI(g)△H=-4.5kJ•mol-1的意义是$\frac{1}{2}$molH2和$\frac{1}{2}$mol I2完全反应生成气态HI放出4.5kJ热量,则1molH2和1mol I2完全反应生成气态HI放出9kJ热量,故C正确;
D.0.5mol H2和0.5mol I2完全反应需要放出4.5kJ热量,不是吸收,故D错误;
故选C.
点评 本题是常识性知识的考查,难度不大.主要是考查学生对热化学方程式含义以及表示的了解掌握情况,旨在培养学生灵活运用基础知识解决实际问题的能力,有利于调动学生的学习兴趣和学习积极性.

练习册系列答案
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案
相关题目
10.已知反应:①Cl2+2KBr═2KCl+Br2;②KClO3+6HCl═3Cl2↑+KCl+3H2O,下列说法正确的是( )
| A. | 上述两个反应都是置换反应 | |
| B. | 反应①中若有1mol Br2生成,则转移电子的物质的量为2mol | |
| C. | 氧化性由强到弱顺序为:KClO3>Cl2>Br2 | |
| D. | 反应②中还原剂与氧化剂的物质的量之比为6:1 |
5.下列不属于天然高分子化合物的是( )
| A. | 淀粉 | B. | 纤维素 | C. | 油脂 | D. | 蛋白质 |
15.从分类的角度来看,下列说法正确的是( )
| A. | 硅酸、氯化铁溶液均为胶体 | B. | 水玻璃、明矾溶液均为混合物 | ||
| C. | 硫酸、纯碱、NaCl分别属于酸、碱、盐 | D. | KCl和Cu均属于电解质 |
2.糖类、油脂、蛋白质和维生素都是人类的基本营养物质,下表为某品牌燕麦片标签中的一部分.
①燕麦片的营养成分中蛋白质水解的产物是氨基酸;等质量的糖类、油脂和蛋白质中提供能量最多的是油脂;人体必需的微量元素是锌,
②维生素C具有的性质是a(填字母).
a.还原性 b.常温下不溶于水 c.溶液显碱性
③苯甲酸钠的作用是防腐剂.
| 每100g含有 营养成分 | 糖类 | 油脂 | 蛋白质 | 维生素C | 钙 | 镁 | 钠 | 锌 | 苯甲酸钠 |
| 7.6g | 7.8g | 7.4g | 18mg | 201mg | 18.2mg | 30.8mg | 8.1mg | -- |
②维生素C具有的性质是a(填字母).
a.还原性 b.常温下不溶于水 c.溶液显碱性
③苯甲酸钠的作用是防腐剂.
20.用Na2SO3溶液吸收硫酸工业尾气中的SO2,Na2SO3+5O2+H2O═2NaHSO3所得混合液可电解循环再生(A为阳离子交换膜;B为阴离子交换膜).相关物料的传输与转化关系如图.下列说法不正确的是( )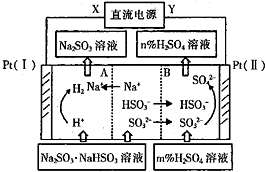

| A. | Pt(Ⅱ)为阳极 | B. | 阳极区[H+]增大 | ||
| C. | 图中的n<m | D. | 阴极电极反应式为2H++2e-═H2↑ |
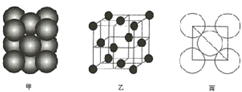 A、B、C、D、E、F为周期表中前36号元素,它们的原子序数依次增大.A元素原子的核外p电子总数比s电子总数少1;B元素原子核外s电子总数与p电子总数相等,且不与A元素在同一周期,C原子最外层电子数是其电子总数的$\frac{1}{3}$;D元素的主族序数与周期数的差为4;E是前四周期中电负性最小的元素;F在周期表的第10列.
A、B、C、D、E、F为周期表中前36号元素,它们的原子序数依次增大.A元素原子的核外p电子总数比s电子总数少1;B元素原子核外s电子总数与p电子总数相等,且不与A元素在同一周期,C原子最外层电子数是其电子总数的$\frac{1}{3}$;D元素的主族序数与周期数的差为4;E是前四周期中电负性最小的元素;F在周期表的第10列.
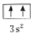 违背了泡利原理.
违背了泡利原理.